A transposição das grandes artérias (TGA) associada a outras anormalidades cardíacas apresenta grandes desafios. Cerca de 30% de todos os casos de TGA apresenta defeito de septo interventricular; por sua vez, a estenose pulmonar é pouco frequente em portadores de septo íntegro, ocorrendo em menos de 5%, além de outras anormalidades da via de saída do ventrículo esquerdo (VSVE), relatadas em até 33% dos pacientes, ilustrando essa expressiva associação1. Daí a importância de saber quais as estratégias podem ser pensadas ao se deparar com tal paciente.
Dentre as alternativas para a correção cirúrgica da TGA com comunicação interventricular (CIV) e obstrução da VSVE, não há um consenso entre os grupos que se dedicam às cardiopatias congênitas. Em geral, o tratamento pode ser subdividido em abordagem ou da via de saída do ventrículo direito (VSVD) ou da VSVE.
Deve-se deixar claro que a operação de Jatene, responsável pelo aumento da sobrevida dos pacientes, principalmente na transposição simples das grandes artérias, não está contraindicada e inclusive deve ser utilizada em casos com anatomia favorável2, encontrando como critério determinante o estudo da VSVE (gradiente ventrículo esquerdo-tronco pulmonar e/ou o fluxo direita-esquerda através da CIV, possibilitando inferir que a obstrução possa não ser tão severa).
Em 1969, Rastelli desenvolveu a ideia que consiste na realização de uma ventriculotomia e tunelização do fluxo do ventrículo esquerdo (VE) para a aorta anterior pelo fechamento de CIV e no redirecionamento do fluxo do ventrículo direito (VD) para o tronco pulmonar por meio da construção de um tubo ventrículo direito-tronco pulmonar (VD-TP)3. Após transeccionar o tronco pulmonar, sua porção proximal é anastomosada a um tubo valvado extracardíaco e este à ventriculotomia, de maneira a estabelecer uma nova VSVD. Sua limitação se deve à tortuosidade da tunelização do VE para a aorta através do VD, estando suscetível à obstrução a médio prazo e à disfunção do tubo valvulado.
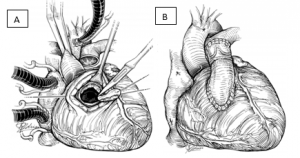
Figura 1. Operação de Rastelli. (A) Tunelização do fluxo VE-aorta. (B) Tubo valvulado anastomosado na ventriculotomia anterior direita.
Fonte: Mavroudis e Backer4.
Um cuidado especial deve ser tomado a fim de não lesar a valva aórtica, que se encontra anterior. A melhor maneira de evitar essa complicação é fazer a ventriculotomia na porção média da parede anterior do VD4. A incisão muscular com a constante visualização da valva aórtica pode ajudar a evadir do dano a essa estrutura. Agora, para o fechamento da CIV, faz-se a configuração de um grande patch com suturas interrompidas e pledgets. Alguns grupos transeccionam a aorta e inserem um dilatador Hagar através da valva para o VE para garantir que nenhuma estenose seja criada pelo patch.
Há diversas relações que interferem na performance desta técnica. Uma artéria coronária cruzando a VSVD determina a realização da ventriculotomia direita mais distal. A presença de CIV de via de entrada ou restritiva ou o straddling da valva mitral ou tricúspide podem revelar grandes obstáculos na criação do túnel intraventricular. Além disso, há uma redução parcial do VD intrínseca ao fechamento da CIV; assim, a presença de hipoplasia direita pode ser uma contraindicação.
A operação de Lecompte ou réparation à l’étage ventriculaire difere da operação de Rastelli pelos reparos intracardíacos por meio da ressecção do septo infundibular que permitem a tunelização mais alinhada, melhorando a VSVE5. O tronco pulmonar, por sua vez, é translocado anteriormente à aorta, por intermédio da manobra de Lecompte e anastomosado diretamente à porção posterior da ventriculotomia direita e feito o fechamento anterior com um patch de pericárdio, com ou sem uma monocúspide.
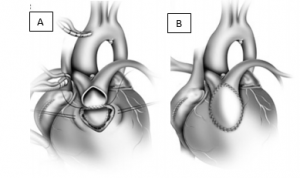
Figura 2. Operação de Lecompte. (A) Tronco pulmonar anterior à aorta. (B) Completa translocação do tronco pulmonar, com fechamento anterior por patch de pericárdio.
Fonte: Cruz et al.6.
Esta técnica tem como vantagens: poder ser realizada em baixa faixa etária; não utilizar os condutos valvulados e permitir o emprego de próteses; poder transformar a operação de Rastelli prévia em decorrência da obstrução do tubo. As desvantagens são: a necessidade de transeccionar a aorta para realizar a manobra de Lecompte; a mobilização e anteriorização da artéria pulmonar também pode causar obstrução da VSVD (para prevenir este problema, Metras et al. descreveram uma modificação desta técnica utilizando um segmento de aorta autográfica para reconstruir a VSVD e mantendo a posição posterior das artérias pulmonares em relação à aorta); além do desafio para a reconstrução da VSVD quando a artéria pulmonar encontra-se lado a lado e à direita da aorta6.
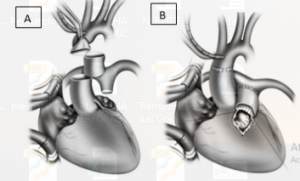
Figura 3. Modificação de Metras. (A) Retirada de um segmento da aorta ascendente. (B) Interposição do segmento entre o tronco pulmonar e o VD.
Fonte: Cruz et al.6.
Em 1984, Nikaidoh et al. propuseram a chamada “translocação aórtica e reconstrução das vias de saída biventriculares”7. Consiste na translocação aórtica com a valva aórtica e artérias coronárias para o VE, após a realização da ampliação da VSVE e fechamento da CIV, posicionando adequadamente a aorta na VSVE. A VSVD é reconstruída com translocação do tronco pulmonar sem a valva pulmonar. Seus pontos-chave são: corrigir de forma anatômica o trajeto VE-aorta; prevenir a estenose de VSVE além de não usar o conduto, diminuindo a incidência de reintervenção na VSVD, em contraste com o procedimento de Rastelli; em comparação com a técnica de Lecompte, previne a obstrução do TP secundária a sua compressão8. A desvantagem está no comprometimento do VD, pelo fato da não preservação da valva pulmonar nativa.
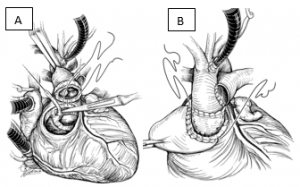
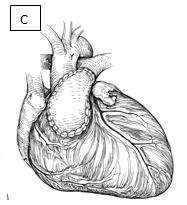
Figura 4. Operação de Nikaidoh. Esquema mostrando a sequência da translocação aórtica, fechamento da CIV e reconstrução da VSVD, sem a preservação da valva pulmonar.
Fonte: Mavroudis e Backer6.
Em 2000, Silva et al. publicaram a chamada “translocação pulmonar”, na qual são mantidas a função da valva pulmonar e a aorta na posição original, sem o risco de manipulação das coronárias ou insuficiência aórtica. Após a construção de um túnel intraventricular para direcionar o fluxo do VE para a aorta, faz-se a translocação da artéria pulmonar para o VD. Os autores usam um pedículo de pericárdio autólogo vascularizado na VSVD, para permitir o potencial crescimento do anel valvar, completando a face anterior da anastomose. Esta cirurgia não elimina a desvantagem de tunelização do VE para a aorta.
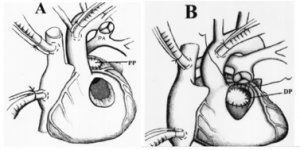
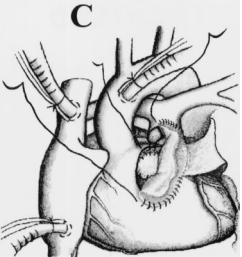
Figura 5. Translocação pulmonar. (A) Dissecção do tronco pulmonar com preservação da valva pulmonar e ventriculotomia direita anterior. (B) Tunelização VE-Ao pelo fechamento da CIV. (C) Reconstrução da VSVD.
Fonte: Da Silva et al.9.
Em 2007, Hu et al. realizaram a translocação da aorta para o VE com a preservação de valva aórtica e artérias coronárias, corrigindo de maneira anatômica a VSVE e reconstruindo a VSVD, com ampliação da valva pulmonar com monocúspide, além da adoção da manobra de Lecompte para anteriorizar a artéria pulmonar. Todavia, no segmento desses pacientes há a disfunção da monocúspide, não eliminando a necessidade de reintervenção da VSVD.
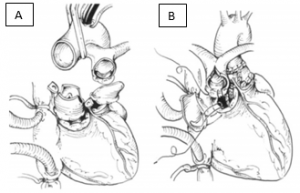
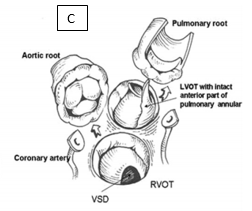
Figura 6. Diagrama mostrando a operação de Nikaidoh modificada. (A) Transecção da aorta e tronco pulmonar (B) Após manobra de Lecompte, reconstrói-se a VSVE, com preservação da valva aórtica. (C) Para ampliar o anel pulmonar com a monocúspide, realiza-se apenas a dissecção da parte posterior do TP.
Fonte: Hu et al.10.
Enaltecendo o brilhantismo da criatividade e capacidade técnica dos cirurgiões brasileiros, em 2010, Furlanetto et al. propuseram uma nova técnica, denominada translocação aórtica e pulmonar, com preservação integral das valvas, que, diferentemente da operação de Nikaidoh, utiliza a valva pulmonar íntegra. Assim, não se realiza a manobra de Lecompte e reduz-se o tempo de pinçamento aórtico, bem como se preserva a função valvar pulmonar, ainda que com estenose moderada.
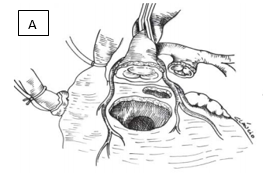
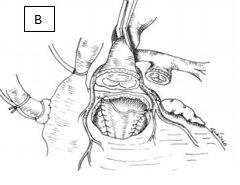
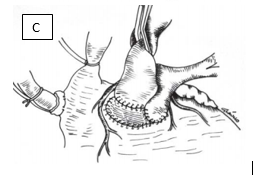
Figura 7. Translocação aórtica e pulmonar. (A) Retirada da aorta e tronco pulmonar, com preservação das valvas nativas. (B) Amplia-se a VSVE e corrige-se a CIV. (C) Finalização da translocação aórtica e pulmonar e o orifício resultante é parcialmente fechado com patch de pericárdio autólogo.
Fonte: Furlanetto et al.11.
A experiência adquirida com as várias operações, pertinentemente constatada com as lesões residuais e reintervenções, não apenas na transposição das grandes artérias, mas também em outras cardiopatias congênitas, permitiu o desenvolvimento de técnicas com a finalidade de obter a maior preservação da anatomia. Destaca-se, pois, que cada procedimento será providencial caso a caso, de modo que a superioridade está contida na máxima: a melhor cirurgia é aquela que teve a indicação mais precisa, ou seja, aquela que for a melhor estratégia, em determinado momento, para determinado paciente.
Referências
- Fyler DC. Report of the New England regional infant cardiac program. Pediatrics. 1980;65(suppl):375-461.
- Jatene IB, Jatene MB. Transposição das grandes artérias. In: Croti UA, Mattos SS, Pinto Jr. VC, Aiello VD, Moreira VM. Cardiologia e cirurgia cardiovascular pediátrica. 2. ed. São Paulo: Roca; 2012. p.529-60.
- Rastelli GC, Wallace RB, Ongley PA. Complete repair of transposition of the great arteries with pulmonary stenosis. A review and report of a case corrected by using a new surgical technique. Circulation. 1969;39(1):83-95.
- Mavroudis C, Backer CL (eds.). Atlas of pediatric cardiac surgery. London: Springer-Verlag; 2015.
- Borromée L, Lecompte Y, Batisse A, Lemoine G, Vouhé P, Sakata R, et al. Anatomic repair of anomalies of ventriculoarterial connection associated with ventricular septal defect. II. Clinical results in 50 patients with pulmonary outflow tract obstruction. J Thorac Cardiovasc Surg. 1988;95(1):96-102.
- Cruz EM, Ivy D, Jaggers J. (eds.). Pediatric and congenital cardiology, cardiac surgery and intensive care. London: Springer-Verlag; 2014.
- Nikaidoh H. Aortic translocation and biventricular outflow tract reconstruction. A new surgical repair for transposition of the great arteries associated with ventricular septal defect and pulmonary stenosis. J Thorac Cardiovasc Surg. 1984;88(3):365-72.
- Mavroudis C, Backer CL (eds.). Pediatric cardiac surgery. 4th ed. Hoboken: Wiley Blackwell; 2013.
- Silva JP, Baumgratz JF, Fonseca L. Pulmonary root translocation in transposition of great arteries repair. Ann Thorac Surg. 2000;69(2):643-5.
- Hu SS, Li SJ, Wang X, Wang LQ, Xiong H, Li LH, et al. Pulmonary and aortic root translocation in the management of transposition of the great arteries with ventricular septal defect and left ventricular outflow tract obstruction. J Thorac Cardiovasc Surg. 2007;133(4):1090-2.
- Furlanetto G, Henriques SS, Pasquinelli FS, Furlanetto BHS. Nova técnica: translocação aórtica e pulmonar com preservação da valva pulmonar. Rev Bras Cir Cardiovasc. 2010;25(1):99-102.