Rodrigo Mendes
Introdução
A dissecção aguda da aorta torácica é uma condição com elevado risco de vida que requer diagnóstico e tratamento imediatos. A dissecção aguda da aorta é a causa mais comum de emergência aórtica. A imagem é essencial para delinear a morfologia e a extensão da dissecção, bem como permitir a classificação (o que determina o manejo). Dois sistemas de classificação são de uso comum, sendo que ambos dividem as dissecções de acordo com o envolvimento da aorta ascendente.1
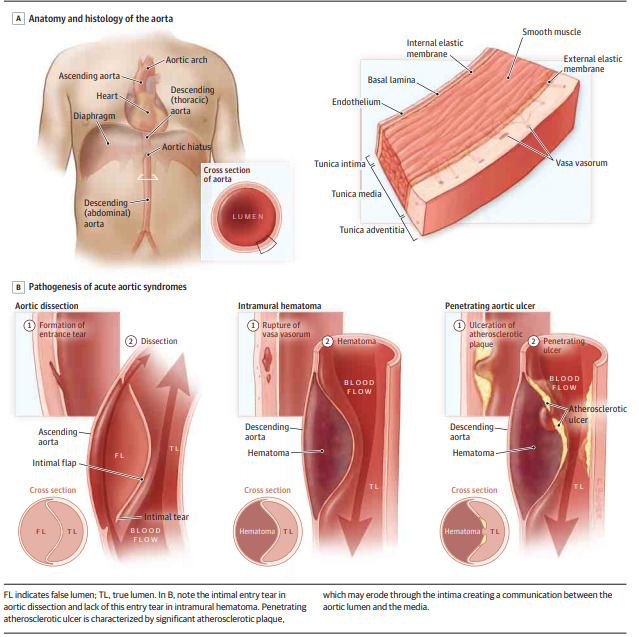
Classificação:
A classificação mais comumente utilizada para dissecções de aorta é o sistema de classificação de Stanford, introduzido em 1970. As dissecções tipo A de Stanford envolvem a aorta ascendente proximal à artéria inominada (tronco braquiocefálico), independentemente da extensão para o arco aórtico ou aorta descendente. As dissecções tipo B de Stanford envolvem apenas a aorta torácica abaixo da artéria subclávia esquerda. A classificação de Stanford não é uma classificação do local da laceração mas o envolvimento dos segmentos da aorta. Consequentemente, uma ruptura da íntima distal à artéria subclávia esquerda com dissecção retrógrada na aorta ascendente será classificada como sendo do tipo A. Por analogia, a ruptura da íntima e a dissecção originadas no arco aórtico serão classificadas como sendo do tipo A se estendendo para a aorta ascendente, e como tipo B se estendendo para a aorta descendente, e como não A não B se contido apenas no arco. De acordo com a classificação DeBakey modificada de 1982, ambas as dissecções DeBakey tipo I e tipo II envolvem a aorta ascendente, mas o tipo I se estende além da artéria inominada, enquanto o tipo II está confinado inteiramente à aorta ascendente. Assim, as dissecções do tipo A de Stanford incluem dissecções de DeBakey do tipo I e do tipo II e as dissecções do tipo B de Stanford são definidas como dissecções do tipo III de DeBakey. A classificação de Stanford é clinicamente útil para orientar o manejo agudo, enquanto a classificação de DeBakey é mais informativa para o acompanhamento de longo prazo, pois diferencia entre envolvimento aórtico proximal e distal.2-4
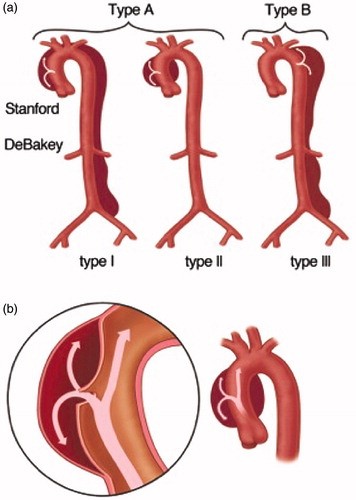
Um novo sistema de classificação foi proposta que é referido pelo acrónimo DISSECT ( D duration – duração, I intimal tear – laceração íntima, S size – tamanho da aorta dissecada, S segmental – segmento, E extent – extensão, C complications – complicações, e T thrombosis – trombose dos falsos lúmen).5
Exames de imagem:
Mais de dois terços dos pacientes requerem pelo menos dois exames de imagem, enfatizando o conceito de que em pacientes de alto risco com um resultado de imagem inicial negativo, é aconselhável realizar um segundo teste para excluir a doença e/ou detalhar a aorta distinta envolvimento do segmento, permitindo o planejamento de tratamento subsequente.6-7
Radiografia de tórax:
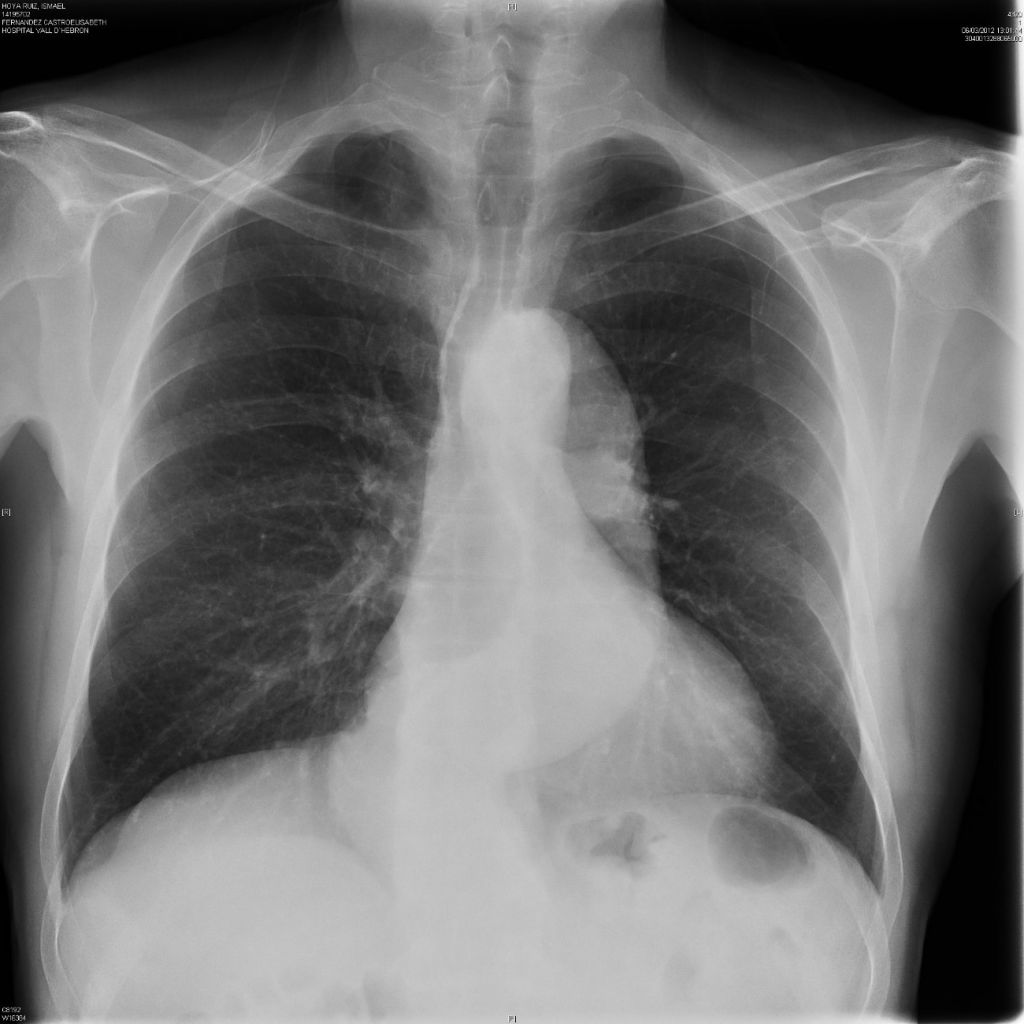
Para lesões do tipo A, a radiografia de tórax pode demonstrar mediastino alargado > 8,0-8,8 cm ao nível do botão aórtico, contorno aórtico duplo, contorno aórtico irregular, deslocamento para dentro da calcificação aterosclerótica (> 1 cm da margem aórtica). Dependendo da etiologia, pode haver sinais de hematoma periaórtico ou mediastinal, que incluem: obscurecimento do botão aórtico, opacificação da janela anteroposterior, desvio das estruturas mediastinais, brônquio principal esquerdo inferiormente (ângulo reduzido da horizontal), aumento da espessura da faixa paratraqueal esquerda e / ou direita, capeamento apical, particularmente à esquerda. Entretanto, 20% a 28% das dissecções não apresentam esse achado. A radiografia não deve ser usada isoladamente para diagnosticar dissecção aórtica.8-12
Tomografia computadorizada (TC)
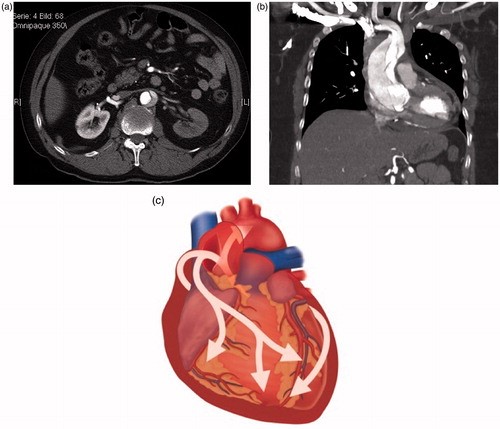
A TC é o método mais rápido, preciso e de maior disponibilidade, para confirmar o diagnóstico de DAT. O objetivo é visualizar os lúmens verdadeiro e falso da aorta durante a dissecção, para identificar rupturas da íntima e avaliar a extensão e o envolvimento dos ramos artérias da aorta. A TC também auxilia no planejamento dos locais de cirurgia e canulação.13-19
A TC também é útil para identificar formas atípicas de doenças agudas da aorta, como hematoma intramural e úlcera aterosclerótica penetrante, que são diagnósticos diferencias de DAT. Essas três entidades são clinicamente indistinguíveis; todas podem cursar com dor torácica ou nas costas em um paciente com hipertensão. A TC também permite a avaliação de outras estruturas toracoabdominais. Uma avaliação completa é especialmente importante para detectar possíveis complicações da dissecção aórtica, como doenças isquêmicas e obstrutivas, que podem aumentar a morbimortalidade. 13-19
Ocasionalmente, em varreduras de TC sem contraste na dissecção aórtica, pode-se ver o deslocamento interno de calcificações da íntima. Esse achado pode ser problemático porque pode ser confundido com um aneurisma com trombo mural calcificado. A alta atenuação do lúmen falso na TC sem contraste pode ajudar a diferenciar as duas condições.13-15
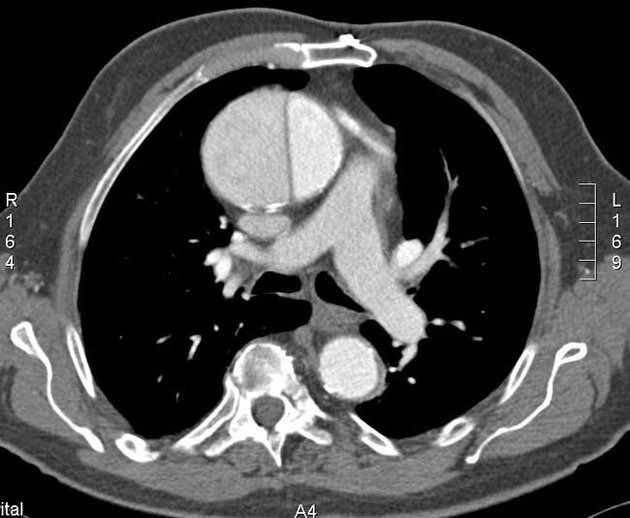
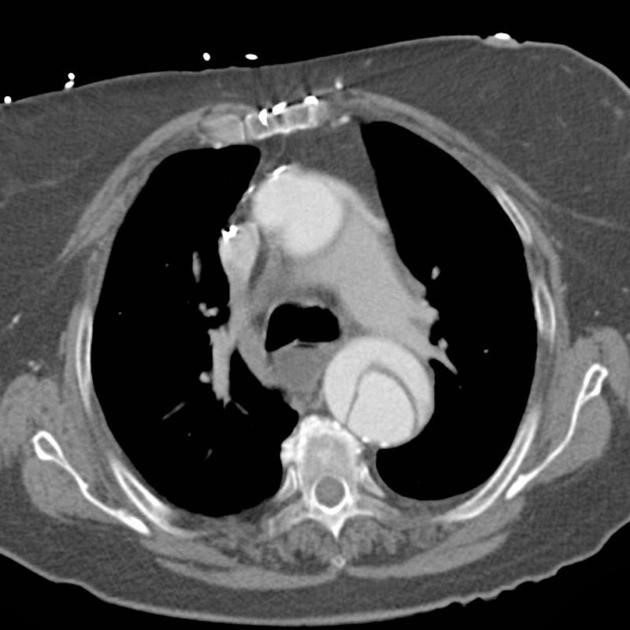
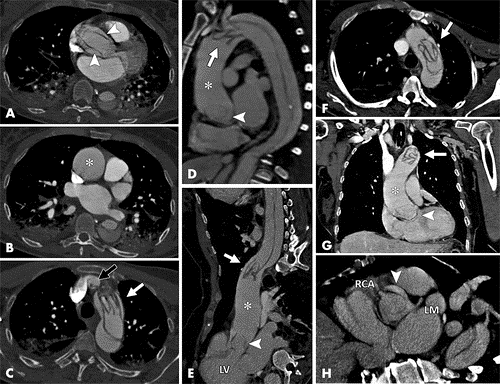
O principal achado em tomografias computadorizadas com contraste de dissecção aórtica é um retalho da íntima que separa o lúmen verdadeiro do falso. A diferenciação precisa na TC entre o lúmen verdadeiro e falso era relativamente sem importância anteriormente porque a cirurgia aberta era a principal terapia usada no tipo B; no entanto, essa distinção tornou-se particularmente importante para o planejamento do tratamento endovascular da dissecção no tipo B. As áreas lineares delgadas de baixa atenuação que ocasionalmente aparecem no lúmen falso nas imagens de TC, conhecidas como sinal da teia de aranha, são específicas do lúmen falso e podem ajudar no seu reconhecimento. Esses achados correspondem a fitas residuais da média, incompletamente seccionadas durante o processo de dissecção. Dois outros indicadores úteis do lúmen falso são uma área transversal maior e o sinal do bico. Este último é a manifestação de imagem em corte transversal da cunha de hematoma que cliva um espaço para a propagação do falso lúmen. Na maioria das tomografias computadorizadas com contraste, entretanto, o lúmen verdadeiro pode ser identificado por sua continuidade com uma porção não dissecada da aorta. 13-19
A intussuscepção da íntima é um tipo incomum de dissecção aórtica produzida pela dissecção circunferencial da camada íntima, que posteriormente invagina como uma biruta – sinal da biruta. A laceração da íntima geralmente começa perto dos óstios coronários. Na intussuscepção da íntima, a tomografia computadorizada pode mostrar um lúmen envolvendo o outro lúmen no arco aórtico, sendo o lúmen medial invariavelmente o lúmen verdadeiro. 13-19
Um aneurisma aórtico com trombo intraluminal pode ocasionalmente ser difícil de distinguir de uma dissecção com um falso lúmen trombosado. O fato de a dissecção geralmente ter formato helicoidal, enquanto o trombo tende a manter uma relação circunferencial constante com a parede aórtica, pode auxiliar na diferenciação visual entre os dois. Além disso, um trombo mural geralmente tem uma borda interna irregular, enquanto uma dissecção geralmente tem uma borda interna lisa. A calcificação íntima que ocorre em um aneurisma aórtico está tipicamente localizada na periferia da aorta. 13-19
O rápido movimento pulsátil da parede aórtica durante o ciclo cardíaco pode produzir estruturas intraluminais lineares falsas nas imagens de TC da aorta ascendente, mimetizando um retalho íntimo (artefatos de pulsação), particularmente em estudos não controlados por eletrocardiograma (ECG).
Ao considerar a angiotomografia, deve-se lembrar que o uso de agentes de contraste iodados leva a um risco não desprezível de reação alérgica e insuficiência renal. No caso de imagens seriadas, ao longo de um período de anos, permanece uma preocupação substancial com o uso de radiação ionizante e o risco de câncer relacionado, que é consideravelmente maior em mulheres e em indivíduos jovens. 13-19
Ressonância nuclear magnética (RNM):
A RNM também fornece altos níveis de precisão diagnóstica na avaliação de pacientes com suspeita de DAT (sensibilidade combinada 98% e especificidade combinada 98%).15-20
Além de informações anatômicas detalhadas sobre a parede do vaso aórtico, a RNM também pode fornecer uma caracterização confiável da insuficiência aórtica tipicamente associada à DAT do Tipo A, incluindo mapeamento de velocidade de contraste de fase para quantificação de fluxo. Além disso, as técnicas angiográficas, podem adicionar informações dinâmicas ao visualizar os padrões de fluxo dentro do lúmen verdadeiro e do lúmen falso. As abordagens mais recentes com a RNM de fluxo 4D mostraram-se promissoras na definição das características de fluxo e dos parâmetros associados da dissecção aórtica, mas precisam ser mais refinados.
Devido ao longo tempo de varredura (20-30 min para o protocolo de avaliação aórtica), a RNM certamente é menos adequada em cenários emergentes ou instáveis do que a TC. Desvantagens adicionais da RNM incluem contra-indicações potenciais, como implantes ferromagnéticos e / ou ativados magneticamente e claustrofobia. Os agentes de contraste à base de gadolínio usados para angiografia com contraste com RNM são definitivamente menos nefrotóxicos do que os agentes iodados, enquanto uma reação adversa grave, como fibrose sistêmica nefrogênica, é extremamente rara e ocorre apenas em pacientes com insuficiência renal avançada.
Quando comparada com a TC, entretanto, a RNM continua sendo excelente opção para imagens de vigilância de doenças aórticas de risco e/ou conhecidas, sem a carga de radiação ionizante e a necessidade de administração intravenosa de agente de contraste iodado. No cenário pós-operatório, o potencial da ressonância magnética para artefatos graves de estruturas como stents aórticos e/ou próteses que obscurecem a visualização do lúmen aórtico também deve ser considerado. Tem sensibilidade e especificidade semelhantes à TC e ETE, mas sofre de disponibilidade limitada e das dificuldades inerentes à realização de ressonância magnética em pacientes instáveis e de locomoção reduzida. 15-20
Ecocardiografia:
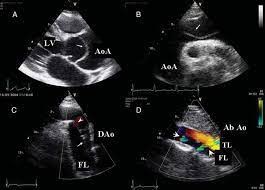
A ecocardiografia transtorácica (ETT) é amplamente utilizada no cenário de emergência como parte de uma abordagem multidisciplinar para o diagnóstico rápido. A ETT avalia o estado funcional do coração, válvulas, raiz aórtica, e segmentos distintos da aorta (visões supraesternal, subcostal e abdominal) e pode mostrar dilatação da aorta, derrame e tamponamento pericárdico, entretanto está associada a pouca visibilidade em obesos, em pacientes com deformidades torácicas e em pacientes em ventilação mecânica, dessa forma, sua precisão para DAT permanece relativamente baixa (sensibilidade de 78-100% para DAT do Tipo A, mas apenas 31–55% para DAT Tipo B). Portanto, um ETT negativo não exclui DAT.21-25
Informações mais detalhadas são obtidas com a ecocardiografia transtorácica (ETE), muito devido à íntima relação entre a aorta e o esofago. A ETE é especialmente útil para detecção de derrame pericárdico e regurgitação da válvula aórtica, e frequentemente identificação da ruptura primária da íntima na raiz da aorta. Em mãos de especialistas, ETE é uma ferramenta de diagnóstico poderosa, e sua sensibilidade e especificidade se aproximam de 100%. As vantagens do ETE em relação à TC e à RNM consistem na possibilidade de ser realizado à beira do leito e/ou na sala operatória sem a necessidade de agentes de contraste de rádio. Por outro lado, é menos adequado do que a TC e a RNM para vigilância por imagem de longo prazo, em que uma avaliação abrangente de toda a aorta e seus vasos ramificados, bem como medições seriadas em pontos de referência facilmente identificáveis, são necessárias.21-25
Outras técnicas:
Ultrassom intravascular
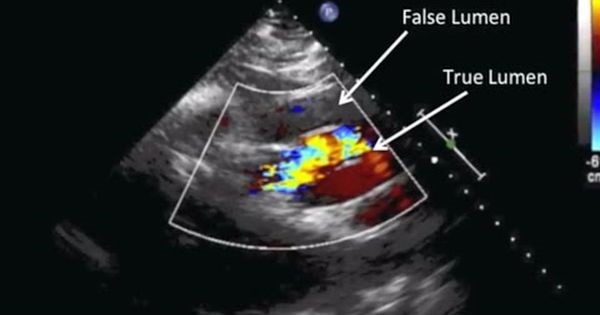
O ultrassom intravascular fornece imagens em tempo real da doença aórtica e é uma ferramenta confiável e segura para orientar o posicionamento da endoprótese. Junto com ETE, pode ser útil para identificar as zonas de aterrissagem, origens de vasos, pontos de cisalhamento, presença de aneurisma sacular e/ou de ulcerações. A imagem intraluminal phased array (também conhecida como ecocardiografia intracardíaca) é uma abordagem alternativa que pode ser implementada para identificar as comunicações entre os lúmens verdadeiros e falsos e para guiar os procedimentos de fenestração.26-27
Tomografia por emissão de pósitrons (PET)
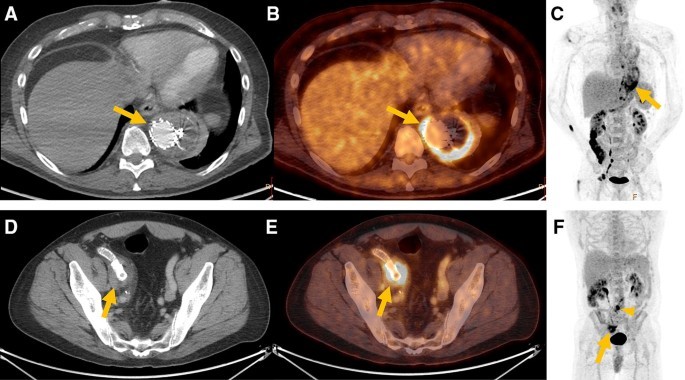
O PET com 18 F-fluorodeoxiglicose ( 18 F-FDG) está desempenhando um papel cada vez mais importante na avaliação de processos inflamatórios e/ou infecciosos da parede aórtica. Atualmente, a aquisição de imagens de angiografia PET/CT ou angiografia por ressonância magnética de modalidade dupla melhorou substancialmente a resolução espacial limitada da PET, fornecendo localização anatômica mais precisa com melhor definição de anormalidades murais ou luminais.28-30
O aumento do sinal de captação 18 F-FDG na parede de uma aorta dissecada, bem como níveis aumentados de marcadores sorológicos de inflamação (dímero D e proteína C reativa) e/ou renovação/lise de trombo (P-selectina, trombina – Complexos de antitrombina III, complexos de plasmina – alfa 2 – antiplasmina e dímero D) podem ter um valor agregado de predição de risco potencial durante o acompanhamento.28-30
Aortografia
A aortografia retrógrada (sensibilidade de até 90% vs. especificidade > 95%) foi o padrão-ouro histórico de diagnóstico para avaliar pacientes com suspeita de DAT. Pela sua natureza invasiva, tempo e custo, raramente é realizada (exceto no caso de angiografia coronariana ou intervenções endovasculares), tendo sido substituída por técnicas de imagem não invasivas.31
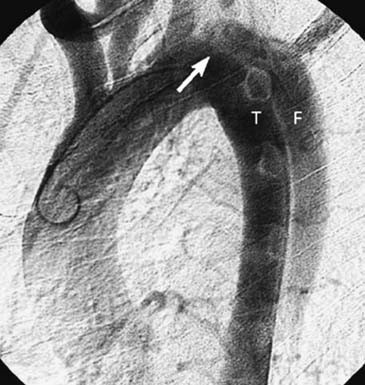
Diagnóstico diferencial
Uma série de entidades que podem simular uma dissecção devem ser consideradas: simples ectasia aórtica, pseudodissecção devido a artefato de movimento de pulsação aórtica (normalmente aspectos anterior esquerdo e posterior direito da aorta ascendente); pseudodissecção devido a faixas de contraste; trombo mural; hematoma intramural – apresentação atípica de dissecção aórtica e parte da síndrome aórtica aguda; úlcera aterosclerótica penetrante que faz parte da síndrome aórtica aguda; atelectasia adjacente; lesão aórtica mínima, etc.31
Complicações
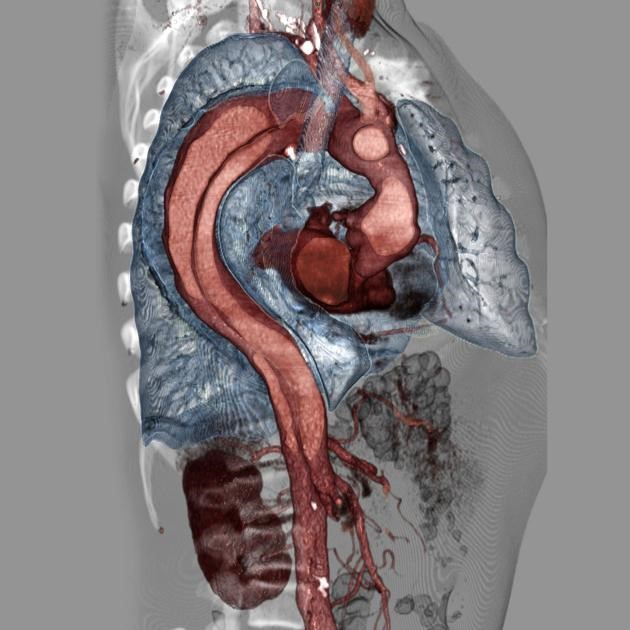
A morte por DAT geralmente é causada por regurgitação aórtica aguda, obstrução de importante ramo, tamponamento pericárdico ou ruptura da aorta. As complicações decorrentes da dissecção da aorta torácica podem ocorrer no tórax ou em localização extratorácica. Mais de um terço dos pacientes com dissecção aórtica apresentam sinais e sintomas secundários ao envolvimento de outros sistemas de órgãos. O mecanismo mais comum é o desenvolvimento de isquemia secundária à obstrução de artérias ramificadas com origem na aorta, como as artérias renais. A obstrução do ramo-vaso pode ser causada por uma extensão do processo de dissecção na parede do vaso ou uma compressão direta da artéria ramo por um lúmen falso em expansão. Outro mecanismo de envolvimento do sistema de órgãos é a ruptura da aorta dissecada, fazendo com que o sangue extravase para as estruturas vizinhas. Esses eventos geralmente são fatais. Portanto, é importante na dissecção da aorta torácica avaliar toda a aorta para determinar a extensão distal da dissecção e detectar possível doença isquêmica abdominal que possa aumentar a morbimortalidade.31
Conclusões
Existem inúmeros métodos
para o estudo radiográfico da DAT, porém a TC deve ser o primeiro teste
diagnóstico realizado quando há suspeita de dissecção aguda da aorta e pode (e deve) ser complementada com outros
métodos, principalment o
ecocadiograma. Os avanços no tratamento percutâneo
tornam importante distinguir entre o lúmen verdadeiro e o lúmen falso no
tipo B; é
essencial conhecer os achados radiológicos na dissecção aórtica e seus diagnósticos
diferenciais. Além disso, toda a aorta deve ser avaliada para determinar a
extensão da dissecção e para identificar possível envolvimento ramo-vaso e
outras eventuais complicações. Mantendo sempre a máxima de um diagnóstico e tratamento rápidos.
Bibliografia:
1. Elsayed RS, Cohen RG, Fleischman F, et al. Acute type A aortic dissection. Cardiol Clin. 2017;35(3):331–345.
2. De Bakey ME, McCollum CH, Crawford ES, et al. Dissection and dissecting aneurysms of the aorta: twenty-year follow-up of five hundred twenty-seven patients treated surgically. Surgery. 1982;92(6):1118–1134.
3. Nienaber CA, Clough RE. Management of acute aortic dissection. Lancet 2015;385(9970):800–811
4. Hagan PG, Nienaber CA, Isselbacher EM, et al. The International Registry of Acute Aortic Dissection (IRAD): new insights into an old disease. JAMA. 2000;283(7):897–903.
5. Dake MD, Thompson M, van Sambeek M, Vermassen F, Morales JP. DISSECT: a new mnemonic-based approach to the categorization of aortic dissection. (2013) European journal of vascular and endovascular surgery : the official journal of the European Society for Vascular Surgery. 46 (2): 175-90.
6. Erbel R, Aboyans V, Boileau C, Bossone E, Bartolomeo RD, Eggebrecht H, Evangelista A, Falk V, Frank H, Gaemperli O, Grabenwöger M, Haverich A, Iung B, Manolis AJ, Meijboom F, Nienaber CA, Roffi M, Rousseau H, Sechtem U, Sirnes PA, Allmen RS, Vrints CJ; ESC Committee for Practice Guidelines . 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases: document covering acute and chronic aortic diseases of the thoracic and abdominal aorta of the adult. The Task Force for the Diagnosis and Treatment of Aortic Diseases of the European Society of Cardiology (ESC). Eur Heart J 2014;35:2873–2926.
7. Hiratzka LF, Bakris GL, Beckman JA, Bersin RM, Carr VF, Casey DEJr, Eagle KA, Hermann LK, Isselbacher EM, Kazerooni EA, Kouchoukos NT, Lytle BW, Milewicz DM, Reich DL, Sen S, Shinn JA, Svensson LG, Williams DM. 2010 ACCF/AHA/AATS/ACR/ASA/SCA/SCAI/SIR/STS/SVM guidelines for the diagnosis and management of patients with thoracic aortic disease: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines, American Association for Thoracic Surgery, American College of Radiology, American Stroke Association, Society of Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, Society of Interventional Radiology, Society of Thoracic Surgeons, and Society for Vascular Medicine. Circulation 2010;121:e266–e369.
8. Bossone E, Suzuki T, Eagle KA, Weinsaft JW. Diagnosis of acute aortic syndromes: imaging and beyond. Herz 2013;38:269–276.
9. de Lacey G, Morley S et-al. The Chest X-Ray: A Survival Guide. Saunders Ltd. ISBN:0702030465.
10. Lai V, Tsang WK, Chan WC et-al. Diagnostic accuracy of mediastinal width measurement on posteroanterior and anteroposterior chest radiographs in the depiction of acute nontraumatic thoracic aortic dissection. Emerg Radiol. 2012;19 (4): 309-15.
11. Gleeson CE, Spedding RL, Harding LA, et al The mediastinum—Is it wide? Emergency Medicine Journal 2001;18:183-185.
12. Gartland S, Sookur D, Lee H. Aortic dissection: an x ray sign. Emerg Med J. 2007;24 (4): 310.
13. Rogers IS, Banerji D, Siegel EL, et al. Usefulness of comprehensive cardiothoracic computed tomography in the evaluation of acute undifferentiated chest discomfort in the emergency department (CAPTURE). Am J Cardiol. 2011;107(5):643–650.
14. Macura KJ, Corl FM, Fishman EK et-al. Pathogenesis in acute aortic syndromes: aortic dissection, intramural hematoma, and penetrating atherosclerotic aortic ulcer. AJR Am J Roentgenol. 2003;181 (2): 309-16
15. Raghupathy A, Nienaber CA, Harris KM, Myrmel T, Fattori R, Sechtem U, Oh J, Trimarchi S, Cooper JV, Booher A, Eagle K, Isselbacher E, Bossone E; International Registry of Acute Aortic Dissection (IRAD) Investigators. Geographic differences in clinical presentation, treatment, and outcomes in type A acute aortic dissection (from the International Registry of Acute Aortic Dissection). Am J Cardiol 2008;102:1562–1566.
16. Grabenwoger M, Alfonso F, Bachet J, Bonser R, Czerny M, Eggebrecht H, Evangelista A, Fattori R, Jakob H, Lonn L, Nienaber CA, Rocchi G, Rousseau H, Thompson M, Weigang E, Erbel R. Thoracic endovascular aortic repair (TEVAR) for the treatment of aortic diseases: a position statement from the European Association for Cardio-Thoracic Surgery (EACTS) and the European Society of Cardiology (ESC), in collaboration with the European Association of Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J 2012;33:1558–1563.
17. Shiga T, Wajima Z, Apfel CC, Inoue T, Ohe Y. Diagnostic accuracy of transesophageal echocardiography, helical computed tomography, and magnetic resonance imaging for suspected thoracic aortic dissection: systematic review and meta-analysis. Arch Intern Med 2006;166:1350–1356.
18. Moore AG, Eagle KA, Bruckman D, Moon BS, Malouf JF, Fattori R, Evangelista A, Isselbacher EM, Suzuki T, Nienaber CA, Gilon D, Oh JK. Choice of computed tomography, transesophageal echocardiography, magnetic resonance imaging, and aortography in acute aortic dissection: International Registry of Acute Aortic Dissection (IRAD). Am J Cardiol 2002;89:1235–1238.
19. Goldstein SA, Evangelista A, Abbara S, Arai A, Asch FM, Badano LP, Bolen MA, Connolly HM, Cuéllar-Calàbria H, Czerny M, Devereux RB, Erbel RA, Fattori R, Isselbacher EM, Lindsay JM, McCulloch M, Michelena HI, Nienaber CA, Oh JK, Pepi M, Taylor AJ, Weinsaft JW, Zamorano JL, Dietz H, Eagle K, Elefteriades J, Jondeau G, Rousseau H, Schepens M. Multimodality imaging of diseases of the thoracic aorta in adults: from the American Society of Echocardiography and the European Association of Cardiovascular Imaging: endorsed by the Society of Cardiovascular Computed Tomography and Society for Cardiovascular Magnetic Resonance. J Am Soc Echocardiogr 2015;28:119–182.
20. Clough RE, Waltham M, Giese D, Taylor PR, Schaeffer T. A new imaging method for assessment of aortic dissection using four-dimensional phase contrast magnetic resonance imaging. J Vasc Surg 2012;55:914–923.
21. Meredith EL, Masani ND. Echocardiography in the emergency assessment of acute aortic syndromes. Eur J Echocardiogr. 2009;10(1):i31–i39.
22. Shiga T, Wajima Z, Inoue T, et al. Survey of observer variation in transesophageal echocardiography: comparison of anesthesiology and cardiology literature. J Cardiothorac Vasc Anesth. 2003;17(4):430–442.
23. Via G, Hussain A, Wells M, Reardon R, ElBarbary M, Noble VE, Tsung JW, Neskovic AN, Price S, Oren-Grinberg A, Liteplo A, Cordioli R, Naqvi N, Rola P, Poelaert J, Guliĉ TG, Sloth E, Labovitz A, Kimura B, Breitkreutz R, Masani N, Bowra J, Talmor D, Guarracino F, Goudie A, Xiaoting W, Chawla R, Galderisi M, Blaivas M, Petrovic T, Storti E, Neri L, Melniker L; International Liaison Committee on Focused Cardiac UltraSound (ILC-FoCUS); International Conference on Focused Cardiac UltraSound (IC-FoCUS). International evidence-based recommendations for focused cardiac ultrasound. J Am Soc Echocardiogr 2014;27:683.e1–683.e33.
24. Neskovic AN, Hagendorff A, Lancellotti P, Guarracino F, Varga A, Cosyns B, Flachskampf FA, Popescu BA, Gargani L, Zamorano JL, Badano LP; European Association of Cardiovascular Imaging. Emergency echocardiography: the European Association of Cardiovascular Imaging recommendations. Eur Heart J Cardiovasc Imaging 2013;14:1–11.
25. Lancellotti P, Price S, Edvardsen T, Cosyns B, Neskovic AN, Dulgheru R, Flachskampf FA, Hassager C, Pasquet A, Gargani L, Galderisi M, Cardim N, Haugaa KH, Ancion A, Zamorano JL, Donal E, Bueno H, Habib G. The use of echocardiography in acute cardiovascular care: recommendations of the European Association of Cardiovascular Imaging and the Acute Cardiovascular Care Association. Eur Heart J Acute Cardiovasc Care 2015;4:3–5.
26. Janosi RA, Gorla R, Rogmann K, Kahlert P, Tsagakis K, Dohle DS, Wendt D, Jakob H, Schlosser T, Bossone E, Erbel R. Validation of intravascular ultrasound for measurement of aortic diameters: comparison with multi-detector computed tomography. Minim Invasive Ther Allied Technol 2015;24:289–295.
27. Bartel T, Eggebrecht H, Müller S, Gutersohn A, Bonatti J, Pachinger O, Erbel R. Comparison of diagnostic and therapeutic value of transesophageal echocardiography, intravascular ultrasonic imaging, and intraluminal phased-array imaging in aortic dissection with tear in the descending thoracic aorta (type B). Am J Cardiol 2007;99:270–274.
28. Kuehl H, Eggebrecht H, Boes T, Antoch G, Rosenbaum S, Ladd S, Bockisch A, Barkhausen J, Erbel R. Detection of inflammation in patients with acute aortic syndrome: comparison of FDG-PET/CT imaging and serological markers of inflammation. Heart 2008;94:1472–1477.
29. Tokuda Y, Oshima H, Araki Y, Narita Y, Mutsuga M, Kato K, Usui A. Detection of thoracic aortic prosthetic graft infection with 18F-fluorodeoxyglucose positron emission tomography/computed tomography. Eur J Cardiothorac Surg 2013;43:1183–1187.
30. Sakalihasan N, Nienaber CA, Hustinx R, Lovinfosse P, El Hachemi M, Cheramy-Bien JP, Seidel L, Lavigne JP, Quaniers J, Kerstenne MA, Courtois A, Ooms A, Albert A, Defraigne JO, 31. Michel JB. (Tissue PET) Vascular metabolic imaging and peripheral plasma biomarkers in the evolution of chronic aortic dissections. Eur Heart J Cardiovasc Imaging 2015;16:626–633.
31. Ko JP, Goldstein JM, Latson LA, Azour L, Gozansky EK, Moore W, Patel S, Hutchinson B. Chest CT Angiography for Acute Aortic Pathologic Conditions: Pearls and Pitfalls. (2021) Radiographics : a review publication of the Radiological Society of North America, Inc. 41 (2): 399-424.
6