Durante o curso da doença valvar aórtica, condições como estenose e insuficiência aórtica podem exigir a troca ou reparo da valva nativa. Dentre as opções disponíveis para troca valvar (implante de prótese mecânica ou biológica, implante percutâneo transcateter, cirurgia de Ross), a cirurgia de Ross é a única que ao garantir o implante de uma valva “viva” em posição aórtica, resulta na viabilidade do substituto valvar a longo prazo. Entretanto, o caráter ousado do procedimento se traduz em maior complexidade em comparação às outras formas de substituição da valva aórtica, além da dificuldade da obtenção do homoenxerto, e por isso, passou a ser uma alternativa pouco frequente para a troca valvar. Apesar das dificuldades técnicas, a cirurgia de Ross apresenta bons resultados a médio e longo prazo, principalmente em pacientes jovens, levando a um renascimento do interesse pelo procedimento.
História
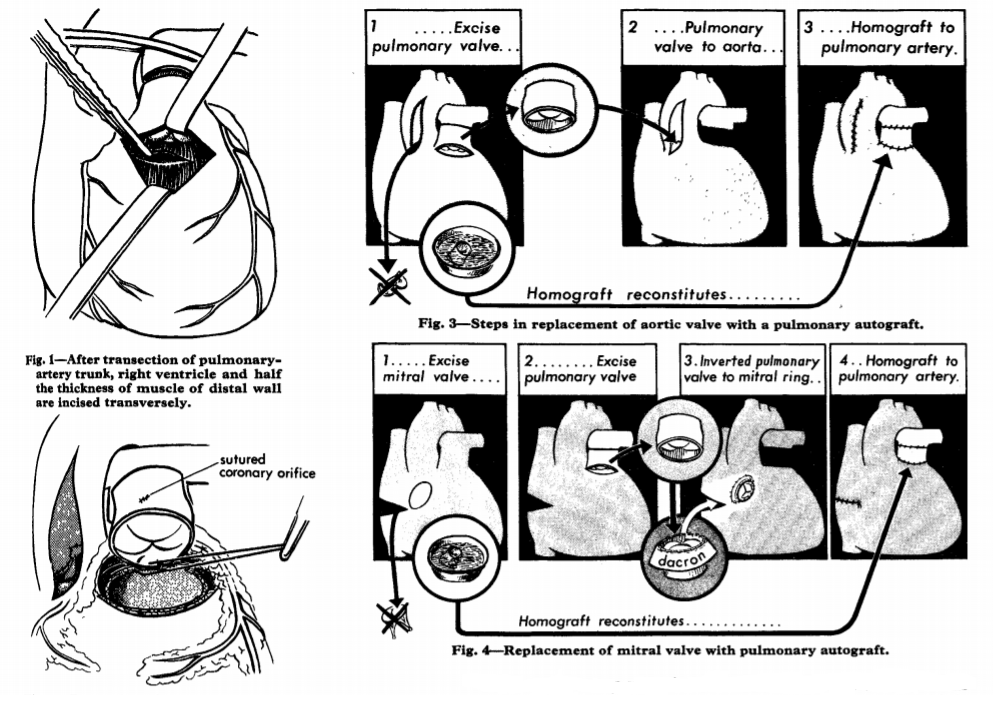
Na história natural da doença valvar aórtica são gerados mecanismos compensatórios, como hipertrofia ou dilatação ventricular, contudo, a falência ventricular é inevitável com a progressão da valvopatia. Assim, na década de 1960, iniciou-se a busca por substitutos valvares que oferecessem um desempenho adequado, e logo foram desenvolvidas as primeiras próteses valvares. Posteriormente, a criação de novas técnicas cirúrgicas de substituição da valva aórtica tinha como objetivo a diminuição do gradiente transvalvar com próteses de fluxo central, e a diminuição dos fenômenos trombogênicos e hemolíticos. Em 1967, a cirurgia de Ross, desenvolvida pelo cirurgião Dr. Donald Ross, foi realizada pela primeira vez em humanos. O procedimento consiste na substituição da valva aórtica pela valva pulmonar do próprio paciente, e esta, por sua vez, é substituída por um homoenxerto. Inicialmente, Dr. Ross e sua equipe realizaram a cirurgia em 14 pacientes, e a experiência inicial foi publicada no periódico The Lancet com a esperança de que o autoenxerto transplantado para posição aórtica se mostrasse competente e durável. No artigo original, foram apresentadas ilustrações demonstrando a técnica cirúrgica executada na época (técnica subcoronariana) (Figura 1). Foram observados 4 óbitos, e nos 10 pacientes restantes, os autoenxertos mostraram-se totalmente competentes durante um período de seguimento de 5 meses2.
Evolução
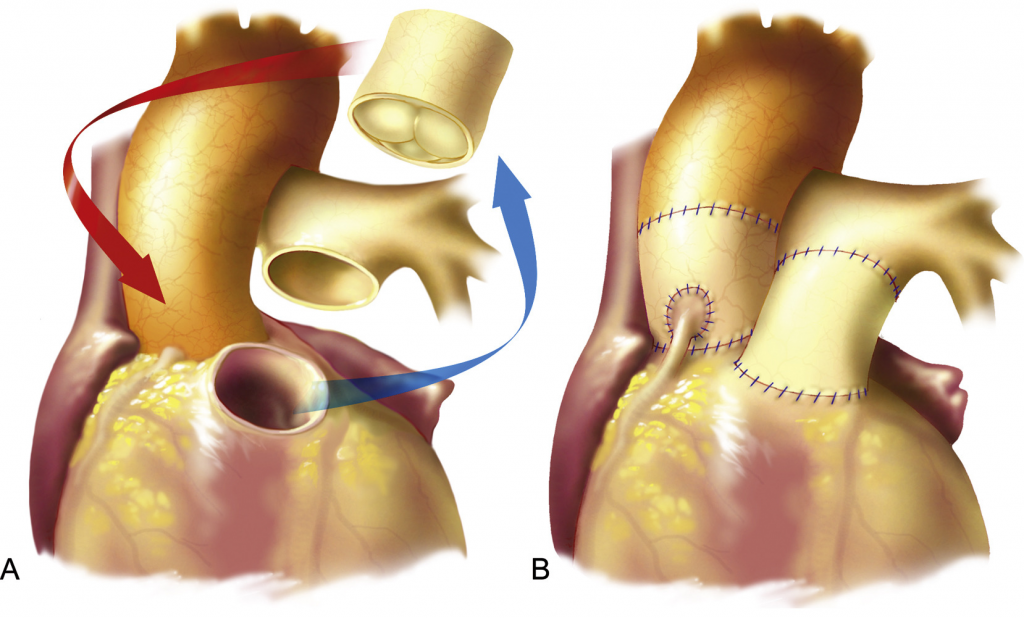
Após sua criação, a técnica da cirurgia de Ross passou por uma série de aprimoramentos a partir da melhor compreensão da anatomia cirúrgica e da dinâmica cardiovascular,4. Originalmente, o autoenxerto era implantado na posição aórtica por meio da técnica subcoronariana. Hoje, a técnica de escolha é a substituição total da “raiz” da aorta, ou seja, a raiz da aorta completa é substituída pelo autoenxerto pulmonar (raiz pulmonar) (Figura 2)4.
Ao longo das últimas décadas, surgiram novos estudos com desenhos metodológicos mais robustos, maior número amostral e tempo de seguimento mais prolongado. Os resultados foram resumidos em uma metanálise recente, e demonstram excelente sobrevida e baixas taxas de tromboembolismo, sangramento e endocardite no período pós-operatório, além de boa viabilidade do autoenxerto com potencial de crescimento (em crianças)5. O autoenxerto proporciona uma hemodinâmica bastante satisfatória, apresentando um gradiente transvalvar muito semelhante ao de uma valva aórtica nativa. Um estudo realizou a avaliação morfológica e funcional da raiz aórtica após diferentes procedimentos de substituição da valva aórtica, e dentre os substitutos valvares investigados (autoenxerto, xenoenxerto e homoenxerto), o autoenxerto foi o substituto mais se aproximou de uma valva aórtica nativa normofuncionante em termos de velocidade máxima6.
O ponto fraco da cirurgia de Ross é o risco aumentado de reintervenções. O maior número de reoperações ocorre, principalmente, na segunda década, e se deve, principalmente, a detalhes técnicos intra-operatórios. As principais razões para reintervenção são a dilatação do autoenxerto pulmonar levando a uma insuficiência aórtica secundária e a estenose do homoenxerto pulmonar3,5. Para mitigar as chances desta evolução, alguns princípios cirúrgicos básicos devem ser seguidos, dentre eles, a estabilização adequada da junção sinotubular. Segundo o German Ross Registry, os resultados a longo prazo do autoenxerto pulmonar com estabilização da junção sinotubular foram consideravelmente superiores em comparação com os resultados do autoenxerto pulmonar sem estabilização7.
Renascimento
Após um período de entusiasmo pelo procedimento na década de 1990, a cirurgia de Ross passou a ser menos realizada. Dentre as motivações para a realização infrequente do procedimento, podem ser apontados a sua complexidade, e o receio de que ambas as valvas (em posição aórtica e pulmonar) apresentassem disfunções em um paciente que, inicialmente, era portador de uma doença valvar única. De fato, os resultados a médio e longo prazo da cirurgia de Ross estão intimamente relacionados à experiência da equipe cirúrgica. Assim, é improvável que resultados altamente satisfatórios possam ser replicados de forma ampla em uma diversidade de instituições.
Contudo, a recente padronização da operação e o conhecimento das etapas críticas do procedimento têm garantido maior reprodutibilidade dos resultados, suscitando um renascimento do interesse pela cirurgia de Ross. A aplicação da técnica de substituição completa da raiz da aorta pelo autoenxerto pulmonar é capaz de propiciar resultados mais padronizados8. Por fim, a adoção mais ampla do procedimento também depende de novos estudos, a fim de suprir limitações como: possível subestimação de eventos relacionados ao autoenxerto visto que a maioria dos estudos já publicados são retrospectivos; e duração do seguimento limitada à primeira década após a cirurgia (a degeneração da valva tem um risco crescente com o tempo).
Referências
- Nakiri K, Stolf NAG, Jatene AD. Próteses valvulares cardíacas. In: Raia A A & Zerbini E J, eds. Clínica cirúrgica Alípio Correa Neto. 4. ed. São Paulo: Sarvier, 1998: vol.3, 756-6
- Ross DN. Replacement of aortic and mitral valves with a pulmonary autograft. Lancet. 1967 Nov 4;2(7523):956-8. doi: 10.1016/s0140-6736(67)90794-5. PMID: 4167516.
- Mazine A, El-Hamamsy I, Verma S, Peterson MD, Bonow RO, Yacoub MH, David TE, Bhatt DL. Ross Procedure in Adults for Cardiologists and Cardiac Surgeons: JACC State-of-the-Art Review. J Am Coll Cardiol. 2018 Dec 4;72(22):2761-2777. doi: 10.1016/j.jacc.2018.08.2200. PMID: 30497563.
- Vojáček J, El-Hamamsy I, Ondrášek J, Žáček P, Fila P, Voborník M, Špatenka J. Current status of the Ross procedure in aortic valve surgery. Cor et Vasa. 2017 51;1: e71-e76. doi: 10.1016/j.crvasa.2017.01.018.
- Etnel JRG, Grashuis P, Huygens SA, Pekbay B, Papageorgiou G, Helbing WA, Roos-Hesselink JW, Bogers AJJC, Mokhles MM, Takkenberg JJM. The Ross Procedure: A Systematic Review, Meta-Analysis, and Microsimulation. Circ Cardiovasc Qual Outcomes. 2018 Dec;11(12):e004748. doi: 10.1161/CIRCOUTCOMES.118.004748. PMID: 30562065.
- Sievers HH et al. A multicentre evaluation of the autograft procedure for young patients undergoing aortic valve replacement: update on the German Ross Registry†. Eur J Cardiothorac Surg. 2016 Jan;49(1):212-8. doi: 10.1093/ejcts/ezv001. Epub 2015 Feb 9. PMID: 25666469.
- Torii R et al. Integrated morphologic and functional assessment of the aortic root after different tissue valve root replacement procedures. J Thorac Cardiovasc Surg. 2012 Jun;143(6):1422-8. doi: 10.1016/j.jtcvs.2011.12.034. Epub 2012 Feb 22. PMID: 22361248.
- Forcillo J, Cikirikcioglu M, Poirier N, El-Hamamsy I. The Ross procedure: total root technique. Multimed Man Cardiothorac Surg. 2014 Oct 8;2014:mmu018. doi: 10.1093/mmcts/mmu018. PMID: 25298364.