O artigo em português “Implementação do Programa de Gerenciamento do Sangue do Paciente: Recomendações Abrangentes e Estratégias Práticas” é a tradução oficial do artigo original em inglês “Patient Blood Management Program Implementation: Comprehensive Recommendations and Practical Strategies“, publicado na edição 39.5 do Brazilian Journal of Cardiovascular Surgery. Essa tradução visa tornar o conteúdo acessível a um público mais amplo, mantendo a integridade das recomendações e estratégias práticas apresentadas no texto original.
Isabel Cristina Céspedes1*, PhD; Maria Stella Figueiredo2, PhD; Nelson Americo Hossne Junior3, PhD; Ítalo Capraro Suriano4, PhD; Rita de Cássia Rodrigues5, PhD; Melca Maria Oliveira Barros2, PhD; Manoel Antonio de Paiva Neto4, PhD; Fernanda Chohfi Atallah6, MSc; Bárbara Burza Benini7, PhD; Adriano Miziara Gonzalez7, PhD; Fábio Veiga de Castro Sparapani4, PhD; Newton de Barros Júnior3, PhD; Ieda Aparecida Carneiro8, PhD; Celina Mayumi Morita Sarto8, MSc; Caio Sussumu de Macedo Motoyama8, PhD; Leonardo Sacchi9; Victor Piovezan8; Simone Luna de Almeida9; Laís da Silva Pereira-Rufino1, PhD; Solange Guizilini3, PhD; Isadora Salvador Rocco3, MSc; Nacime Salomão Mansur8, MSc; Jaquelina Sonoe Ota Arakaki10, PhD; Antonio Alceu dos Santos11, PhD; Carlos Eduardo Panfilio12, PhD
1Departamento de Morfologia e Genética, Disciplina de Genética, Escola Paulista de Medicina, Universidade Federal de São Paulo (UNIFESP), São Paulo, São Paulo, Brasil.
2Departamento de Oncologia Clínica e Experimental, Disciplina de Hematologia e Hemoterapia, Escola Paulista de Medicina, Universidade Federal de São Paulo (UNIFESP), São Paulo, São Paulo, Brasil.
3Departamento de Cirurgia, Disciplina de Cirurgia Cardiovascular, Escola Paulista de Medicina, Universidade Federal de São Paulo (UNIFESP), São Paulo, São Paulo, Brasil.
4Departamento de Neurologia e Neurocirurgia, Disciplina de Neurocirurgia, Escola Paulista de Medicina, Universidade Federal de São Paulo (UNIFESP), São Paulo, São Paulo, Brasil.
5Departamento de Anestesiologia, Dor e Cuidados Intensivos, Disciplina de Anestesiologia, Escola Paulista de Medicina, Universidade Federal de São Paulo (UNIFESP), São Paulo, São Paulo, Brasil.
6Departamento de Anestesiologia, Dor e Cuidados Intensivos, Disciplina de Medicina Intensiva, Escola Paulista de Medicina, Universidade Federal de São Paulo (UNIFESP), São Paulo, São Paulo, Brasil.
7Departamento de Cirurgia, Disciplina de Gastroenterologia Cirúrgica, Escola Paulista de Medicina, Universidade Federal de São Paulo (UNIFESP), São Paulo, São Paulo, Brasil.
8Hospital São Paulo, Hospital Universitário da Universidade Federal de São Paulo (UNIFESP), São Paulo, São Paulo, Brasil.
9Departamentos de Suprimentos e Farmácia. Associação Paulista para o Desenvolvimento da Medicina (SPDM), São Paulo, São Paulo, Brasil.
10Departamento de Medicina, Disciplina de Pneumologia, Escola Paulista de Medicina, Universidade Federal de São Paulo (UNIFESP), São Paulo, São Paulo, Brasil.
11Departamento de Oncologia Clínica e Experimental, Programa de Pós-graduação em Medicina – Hematologia e Oncologia, Escola Paulista de Medicina, Universidade Federal de São Paulo (UNIFESP), São Paulo, São Paulo, Brasil.
12Escola da Saúde, Universidade Municipal de São Caetano do Sul (USCS), São Caetano do Sul, São Paulo, Brasil.
Este estudo foi realizado no Departamento de Morfologia e Genética, Escola Paulista de Medicina, Universidade Federal de São Paulo, São Paulo, São Paulo, Brasil.
* Autor de correspondência:
Isabel Cristina Céspedes
https://orcid.org/0000-0003-4806-3548
Rua Botucatu, 740 – 1º andar – Edifício Leitão da Cunha, São Paulo, SP, Brasil
CEP: 04023-062
E-mail: isabel.cespedes@unifesp.br
Artigo recebido em 19 de junho de 2024.
Artigo aceito em 27 de junho de 2024.
Abreviações, Acrônimos e Símbolos
CEC = Circulação Extracorpórea
EPM = Escola Paulista de Medicina
EPO = Eritropoetina
FDL = Filtro de depleção de leucócitos
Hb = Hemoglobina
HU = Hospital São Paulo
ISS = Injury Severity Score ou Índice de Gravidade da Lesão
IV = Intravenoso
PBM = Patient Blood Management (Gerenciamento do Sangue do Paciente)
RNI = Razão Normalizada Internacional
SC = Subcutâneo
SUS = Sistema Único de Saúde
TCA = Tempo de coagulação ativado
TTP = Tempo de tromboplastina parcial
UNIFESP = Universidade Federal de São Paulo
UTI = Unidade de Terapia Intensiva
RESUMO
Introdução: A transfusão de sangue é uma das práticas médicas mais comuns em todo o mundo. No entanto, a literatura científica atual tem demonstrado que os efeitos imunomodulatórios da transfusão sanguínea estão associados a maior chance de infecção, maior tempo de internação e morbimortalidade. Além disso, ela implica em custos elevados para os sistemas de saúde.
Métodos: Nesse contexto, reconhecendo que as transfusões de sangue são, essencialmente, um transplante heterólogo de células, o uso de opções terapêuticas vem ganhando força e seu conjunto é conhecido como programa de Gerenciamento do Sangue do Paciente (PBM). O PBM é uma abordagem baseada em três pilares principais: (1) tratamento de anemias e coagulopatias de forma otimizada, especialmente no período pré-operatório; (2) otimização da hemostasia perioperatória e uso de sistemas de recuperação sanguínea para evitar a perda do sangue do paciente; (3) tolerância à anemia, com maior oferta e redução da demanda de oxigênio, principalmente no período pós-operatório.
Resultados: As evidências científicas atuais apoiam a eficácia do PBM em reduzir a necessidade de transfusões sanguíneas, diminuir as complicações associadas e promover um manejo mais eficiente e seguro do sangue. Assim, o PBM não só melhora os resultados clínicos dos pacientes, mas também contribui para a sustentabilidade econômica dos sistemas de saúde.
Conclusão: O objetivo desta revisão foi sumarizar as estratégias do PBM em uma abordagem abrangente e baseada em evidências, por meio de um modelo sistemático e estruturado para a implementação do PBM em hospitais terciários. As recomendações aqui propostas são de pesquisadores e especialistas de um hospital universitário de alta complexidade da rede do Sistema Único de Saúde, apresentando-se como uma estratégia que pode ser seguida como diretriz para a implementação em outros cenários.
Palavras-chave: transfusão de sangue, diretriz, estratégias de saúde, hospitalização, custo e análise de custos, pessoal de pesquisa, centros de atenção terciária, saúde pública.
INTRODUÇÃO
Historicamente, a transfusão de sangue alogênico se tornou uma das práticas médicas mais comuns em todo o mundo, em grande parte devido ao seu desenvolvimento e uso generalizado durante as Guerras Mundiais[1]. Infelizmente, ela tem sido prescrita sem a devida avaliação por parte dos médicos, supostamente motivados pela baixa prevalência e severidade das reações transfusionais, principalmente aquelas de maior gravidade, sugerindo se tratar de um recurso terapêutico totalmente seguro. Porém, o avanço de métodos científicos moleculares tem identificado efeitos cada vez mais deletérios das transfusões sanguíneas naqueles que as recebem, que resultam em maior morbidade e mortalidade. A imunomodulação relacionada à transfusão de sangue alogênico (transfusion-related immunomodulation) traz consequências significativas ao paciente por meio de mecanismos ainda não totalmente compreendidos. Esses mecanismos têm sido associados à diminuição da função das células natural killer e das células apresentadoras de antígenos, à redução da imunidade mediada por células e ao aumento das células T reguladoras[2]. Por meio desses efeitos imunomoduladores e inflamatórios, as transfusões de sangue alogênico têm sido associadas a maior risco de infecção, maior tempo de internação e aumento da morbidade e mortalidade, independentemente da presença de fatores confundidores como características demográficas, equipe de saúde, infraestrutura hospitalar e condições do paciente[1,3].
Além disso, com o envelhecimento da população, é esperada uma significativa redução nos estoques dos bancos de sangue, o que implicará à Medicina trabalhar sem transfusões de sangue alogênico em muitos cenários[4]. Adicionalmente, as transfusões de sangue alogênico representam altos custos para os sistemas de saúde, quando contabilizamos a sua produção, transporte, armazenamento e administração hospitalar. O ônus desses custos por unidade de sangue é assumido não só pelo sistema público de saúde (Sistema Único de Saúde [SUS] no Brasil), mas também por entidades privadas de saúde. A permanência hospitalar prolongada e as morbidades associadas às transfusões de sangue alogênico aumentam ainda mais esses custos [5]. Em 2023, a Joint Commission relatou que em hospitais americanos, 86,48% das transfusões foram inapropriadas ou desnecessárias, ao custo de milhões de dólares[6].
Nesse contexto, estratégias que visam reduzir ou eliminar o uso de transfusões de sangue alogênico devem ser implementadas. Elas são coletivamente conhecidas como Gerenciamento do Sangue do Paciente (Patient Blood Management – PBM), com recomendações aplicadas a pacientes clínicos e cirúrgicos. Para pacientes cirúrgicos, essas estratégias são agrupadas em três pilares de acordo com o período perioperatório: pré-operatório, intraoperatório e pós-operatório. Esquemas simplificados dessas estratégias podem ser encontrados nos artigos de Farmer et al.[4] ou de Santos et al.[7].
Um exemplo bem-sucedido de implementação do PBM foi observado na Austrália, com redução no uso de hemocomponentes (41% de concentrado de hemácias, 47% de plasma e 27% de concentrado de plaqueta), resultando em redução de 28% no índice de mortalidade, 31% no infarto agudo do miocárdio/acidente vascular cerebral, 15% no tempo de internação e 21% na taxa de infecção, associado a economia de aproximadamente 100 milhões de dólares australianos em custos diretos e indiretos[8]. Depois de 20 anos de implementação bem-sucedida do PBM no Canadá, reduções significativas no tempo de internação e nas taxas de infecção foram observadas em cirurgia cardíaca e ortopédica, economizando cerca de 50 milhões de dólares canadenses por ano[9].
Em 2021, a Organização Mundial da Saúde (OMS) declarou que a implementação do PBM nos hospitais em todo o mundo é uma necessidade urgente[8].
Portanto, o objetivo da presente revisão foi sumarizar as estratégias do PBM usando uma abordagem abrangente e baseada em evidências, por meio de um modelo sistemático e estruturado para implementação do PBM em hospitais terciários.
Pilares do PBM
O PBM é um programa que engloba vários modelos e estratégias, dependendo dos autores ou das diretrizes utilizadas, geralmente apresentados como constituindo três pilares[4,7]:
– 1º pilar (foco no período pré-operatório) – otimizar a massa eritrocitária e a coagulação: envolve primariamente o tratamento de anemias e coagulopatias e o preparo do paciente para procedimentos cirúrgicos, incluindo aspectos nutricionais.
– 2º pilar (foco no período intraoperatório) – minimizar a perda sanguínea: envolve preservar o sangue do paciente, minimizar sua perda durante a cirurgia e otimizar a coagulação e hemostasia cirúrgica através do uso de hemostáticos tópicos e sistêmicos, instrumentos hemostáticos cirúrgicos, recuperação de células sanguíneas e/ou hemodiluição normovolêmica aguda.
– 3º pilar (foco no período pós-operatório) – tolerância à anemia: envolve o conceito de tolerância à anemia por meio de medidas que visam melhorar o fornecimento de oxigênio aos tecidos, sedação e otimização da analgesia para reduzir o consumo de oxigênio, minimizar a frequência e o volume das flebotomias, manutenção da normotermia e otimização do débito cardíaco com expansores de volume, quando apropriado.
No Brasil, a maioria das estratégias de diagnóstico, dos tratamentos farmacológicos (para anemias, coagulopatias, hemostasia, kits de equipamentos) e dos equipamentos necessários (recuperação de células sanguíneas, testes viscoelásticos) para a implementação do PBM está incluída na Relação Nacional de Medicamentos (RENAME) e na Relação de Equipamentos e Materiais (RENEM) do SUS, o que garante a viabilidade de sua implementação nos hospitais[7].
É importante ressaltar que o PBM representa uma mudança de paradigma que reconhece a transfusão de hemocomponentes como um transplante de tecido heterólogo, com todas as suas implicações e complicações, e não deve ser confundido com estratégias transfusionais restritivas ou meramente com o tratamento de anemias.
MÉTODOS
Proposta para Implementação do PBM
A recomendação para implementar o PBM surgiu de uma iniciativa de gestores, especialistas e pesquisadores da Escola Paulista de Medicina (EPM) / Universidade Federal de São Paulo (UNIFESP) / Hospital São Paulo (HU/UNIFESP). À medida que esses profissionais se aprofundavam no assunto, eles reconheciam sua relevância destacando principalmente a maior segurança para o paciente, o uso eficiente dos recursos financeiros da saúde pública e a preocupação com o adiamento de procedimentos cirúrgicos devido à escassez de hemocomponentes nos bancos de sangue. Além disso, eles consideraram o envelhecimento da população brasileira, o que deverá reduzir ainda mais a disponibilidade de doadores, juntamente com potenciais novas pandemias de transmissão sanguínea que possam surgir.
Recomendação do Passo a Passo para Implementação: Plano de 10 passos
1º passo – Iniciativa: Motivadores Individuais
Muitos gestores médicos e não-médicos, hematologistas, clínicos, cirurgiões, obstetras, anestesiologistas, intensivistas, enfermeiros, biomédicos e outros profissionais da saúde podem ter sido apresentados ao PBM e aos argumentos convincentes que apoiam sua implementação urgente. Esse primeiro passo envolve abordar a equipe de gestão do hospital e/ou parceiros estratégicos como agências transfusionais, e/ou chefes de áreas cirúrgicas, de unidades de terapia intensiva (UTIs) ou anestesiologia, para apresentar o assunto e identificar possíveis caminhos para a implementação do PBM em seu contexto hospitalar.
2º passo – Criar um Grupo de Trabalho
A implementação de um programa de PBM, independentemente da descrição aqui apresentada como uma estratégia em etapas, envolve o cuidado contínuo e global do paciente e, portanto, vários setores do ambiente hospitalar. Além disso, envolve vários aspectos como a definição das áreas onde ele deve ser implementado, o desenvolvimento de protocolos e processos bem estabelecidos, e o monitoramento e auditoria do progresso da implementação — incluindo ajustes quando necessário — e requer a consolidação de um Grupo de Trabalho representativo de diversos setores do hospital. Esse Grupo de Trabalho pode se tornar um grupo assessor permanente e contínuo.
3º passo – Definir as Áreas-Piloto
Após sua formação, o Grupo de Trabalho deve identificar uma ou duas áreas cirúrgicas (piloto) para a implementação do PBM. Essa abordagem permite que esforços sejam concentrados nas áreas que podem servir como modelos internos e de acreditação. A seleção deve ser baseada em considerações técnicas e na disposição de áreas específicas em assumir os esforços iniciais para a implementação e mudança de paradigmas.
4º passo – Diagnóstico Local: Conhecimento, Infraestrutura e Pessoal
Após a formação do Grupo de Trabalho e a seleção das áreas-piloto, ações claras e objetivas devem ser planejadas para envolver as principais partes interessadas e os ambientes incluídos na implementação do PBM, com foco em médicos, enfermeiros e administradores. Portanto, é necessário um diagnóstico do local, que pode ser realizado por meio perguntas claras e objetivas em formato eletrônico.
Esse questionário deve incluir perguntas sobre:
- a) como as equipes analisam criticamente os riscos e benefícios das transfusões de sangue alogênico antes de prescrevê-las e administrá-las, seu conhecimento sobre PBM e sua disposição em mudar sua prática; e
- b) a infraestrutura local disponível em termos de testes diagnósticos, medicações (para anemias, coagulopatias, sangramento), equipamentos (recuperação de células sanguíneas, testes viscoelásticos) e recursos humanos que o hospital possui.
5º passo – Sensibilizar e Capacitar
Com base no nível de conhecimento identificado através da avaliação do item “a” do 4º passo, promover: i) um ou mais encontros com equipes das áreas-piloto para alinhá-las com a implementação do PBM; ii) cursos de capacitação sobre ações práticas na implementação do PBM. Esse passo é de fundamental importância. Se houvesse treinamento em PBM desde a graduação ou um programa de capacitação institucionalizado, o PBM já estaria naturalmente integrado às rotinas médicas e hospitalares, reduzindo significativamente muitos dos atuais esforços de implementação. A educação é, de fato, a principal força motriz para que o PBM tenha efeito.
6º passo – Definir as Estratégias do PBM e Criar Protocolos
Cada ambiente hospitalar tem suas características, pontos fortes e desafios na implementação do PBM, os quais podem ser identificados através da avaliação do item “b” do 4º passo. Portanto, com base nas possíveis estratégias de PBM sugeridas por Farmer et al.[4] e Santos et al.[7], o Grupo de Trabalho deve discutir e definir quais delas incorporar localmente. Deve-se considerar não só a infraestrutura e os recursos humanos disponíveis, mas também o quanto a gestão hospitalar está disposta a investir nessas dimensões, considerando que o programa PBM diminuirá significativamente os custos por meio da redução do uso de hemocomponentes e de menos complicações clínicas, entre outros. Devem ser desenvolvidos protocolos assistenciais para as estratégias do 1º pilar (manejo de anemias e coagulopatias), 2º pilar (uso de hemostáticos tópicos e sistêmicos, recuperação de células sanguíneas, hemodiluição normovolêmica aguda, testes viscoelásticos) e 3º pilar (tolerância e manejo da anemia e do sangramento pós-operatório com o uso de testes viscoelásticos para identificar as causas). Essa também é uma etapa crucial para a implementação eficaz do PBM no mundo real. Esses protocolos assistenciais provenientes de estudos baseados em evidências proporcionam a tomada de decisão imediata, precisa e prática.
7º passo – Definir uma Data de Início
Assegurar-se de que todas as etapas anteriores estejam consolidadas e definir um mês de início para a implementação, para coletar dados retrospectivos (pré-PBM) e prospectivos (pós-PBM).
8º passo – Reuniões Quinzenais
É necessário o monitoramento rigoroso das ações de implementação do PBM por meio de análises SWOT (Strengths, Weaknesses, Opportunities, and Threats) ou FOFA (pontos fortes, oportunidades, fraquezas e ameaças), assim como ajustes e adaptações contínuos.
9º passo – Avaliar os Resultados
Por meio de prontuários eletrônicos ou banco de dados do hospital, obter dados anônimos sobre os principais resultados a serem analisados após a implementação do PBM, como índices globais sobre a quantidade e o tipo de hemocomponentes usados no período perioperatório, taxas de infecção, tempo internação no pós-operatório, reoperações, marcadores inflamatórios, complicações pós-operatórias e mortalidade na área implementada.
10º passo – Auditoria de Conformidade e Resultados
Além das avaliações técnicas e financeiras diretamente relacionadas à implementação controladas pelo Grupo de Trabalho, para garantir a eficácia e a adesão à implementação do PBM recomendam-se auditorias regulares e sistemáticas através de um Comitê Consultivo formado dentro do Grupo de Trabalho (com pelo menos dois de seus membros), incluindo um representante do setor de segurança do paciente ou do setor de qualidade do hospital e um representante da diretoria administrativa. Essas auditorias devem incluir:
– Definição de indicadores de desempenho: estabelecer indicadores claros e mensuráveis como, por exemplo, redução do uso de hemocomponentes, diminuição das complicações pós-operatórias, redução do tempo de internação hospitalar, redução das taxas de infecção, redução dos índices de mortalidade e análise de custo-efetividade. Este trabalho pode ser realizado em colaboração com o Grupo de Trabalho.
– Monitoramento contínuo: implementar um sistema de monitoramento contínuo para acompanhar os indicadores de desempenho, permitindo a identificação oportuna de desvios e ações corretivas subsequentes.
– Avaliação de conformidade pela condução de auditorias periódicas: realizar auditorias periódicas para verificar a adesão às diretrizes do PBM, incluindo a revisão de prontuários médicos, a análise de protocolos clínicos e a observação direta das práticas transfusionais.
– Feedback e melhoria contínua: estabelecer um mecanismo de feedback envolvendo as equipes de saúde e administrativa, promovendo a melhoria contínua com base nos resultados das auditorias e nas melhores práticas identificadas.
– Relatórios de desempenho: elaborar relatórios regulares resumindo os resultados das auditorias e do monitoramento, destacando as áreas de sucesso e as oportunidades de melhora.
Implementando essas etapas de auditoria e conformidade, será possível garantir que o PBM seja aplicado de forma eficaz, seguindo as diretrizes estabelecidas, promovendo a segurança do paciente e a eficiência na utilização dos recursos de saúde.
Observe que os passos recomendados para a implementação do PBM podem mudar pois, alguns deles, podem ocorrer simultaneamente ou em múltiplas etapas, dependendo da dinâmica ou dos desafios de cada local.
RESULTADOS
Ações Estratégicas na Implementação do PBM – Práticas Eficientes
Com base na recomendação passo a passo descrita anteriormente, o Grupo de Trabalho conhecido como PBM-HU-UNIFESP (https://pbm.unifesp.br/), responsável pela implementação do PBM no HU/UNIFESP, após análise abrangente da literatura científica atual e após intensas discussões entre os especialistas e as áreas envolvidas, recomenda a aplicação das seguintes práticas:
No que diz respeito ao 1º. passo e ao papel inicial dos motivadores individuais na superação dos desafios para a implementação do PBM, é essencial que uma liderança motivada e dedicada, com expertise em PBM, acione a diretoria clínica do hospital, que deve desempenhar um papel ativo, facilitando as discussões iniciais e servindo como um elo entre as áreas potenciais e seus representantes. Neste caso, por exemplo, a EPM/UNIFESP contou com a iniciativa de uma liderança de seu corpo docente.
A recomendação prática para o 2º. passo é estabelecer um Grupo de Trabalho, considerando a necessidade crucial de colaboração multidisciplinar para viabilizar o PBM e garantir que todas as perspectivas e preocupações sejam abordadas. Como no exemplo do Grupo PBM-HU-UNIFESP, esse Grupo de Trabalho deve incluir membros da Comissão Transfusional e chefes/representantes da área de Hematologia/Hemoterapia focando no 1º pilar; chefes/representantes inicialmente de uma ou duas áreas Cirúrgicas e da Anestesiologia focando no 2º pilar; e coordenadores/representantes das unidades de terapia intensiva (UTIs) focando no 3º pilar. Importante para todos os pilares, o Grupo de Trabalho deve incluir a direção da Enfermagem, o setor de suprimentos (devido às demandas por testes diagnósticos e medicamentos para anemias, coagulopatias, hemostasia e kits descartáveis para equipamentos), a engenharia clínica (para garantir a viabilidade e manutenção de equipamentos como a máquina de recuperação de células sanguíneas e testes viscoelásticos), e um representante da residência médica. Esse grupo tem o potencial de se expandir à medida que o PBM se estende para áreas além daquelas inicialmente envolvidas e, idealmente, deve ser permanente e integrado à direção clínica do hospital.
Para o 3º passo é recomendado, como no exemplo prático do Grupo PBM-HU-UNIFESP, que duas áreas cirúrgicas sejam inicialmente selecionadas como áreas-piloto de implementação (em nossa implementação, cirurgia cardiovascular e neurocirurgia). Duas áreas-piloto permitem a identificação da origem de possíveis dificuldades, sejam elas relacionadas ao PBM ou, especificamente, àquela área cirúrgica. A triagem e seleção dessas áreas-piloto devem incluir aquelas com alto risco de perda sanguínea perioperatória e aquelas que demonstrem interesse imediato em facilitar essa fase inicial. A experiência adquirida nessas áreas-piloto permite um avanço estruturado em outras áreas, garantindo uma implementação gradual e bem-sucedida do PBM em todo o hospital.
Para o 4º passo recomenda-se que o Grupo de Trabalho entenda completamente o cenário do hospital em relação ao PBM e seus aspectos técnicos e administrativos. Como no exemplo do Grupo PBM-HU-UNIFESP, devem ser utilizadas ferramentas de avaliação abrangentes, como questionários cientificamente embasados e de fácil utilização (perguntas de múltipla escolha com espaço para o detalhamento das respostas). Esses questionários devem ser aplicados eletronicamente às equipes de saúde das áreas-piloto e incluir perguntas sobre: a) conhecimento sobre a prática transfusional e sobre o PBM com base em seus princípios; e b) infraestrutura e pessoal disponíveis, conforme as diretrizes do manual de acreditação hospitalar (Manual Brasileiro de Acreditação Hospitalar; Brasil)[10]. A análise das informações obtidas identificará a necessidade de treinamento e as dificuldades, especialmente em relação ao uso de transfusões de sangue alogênico e às práticas do PBM. Estudos mostram que há treinamento insuficiente em medicina transfusional e PBM nas escolas médicas do Brasil e do mundo[11,12]. Seguindo a experiência do Grupo PBM-HU-UNIFESP, essa ferramenta de avaliação pode ser disponibilizada por meio de convênios ou parcerias com instituições interessadas, facilitando a identificação das necessidades específicas do hospital e permitindo um planejamento futuro mais preciso e eficaz. Utilizar essas ferramentas é fundamental para adequar o PBM às especificidades de cada instituição, promovendo melhores resultados clínicos e operacionais.
A recomendação prática para o 5º passo é diagnosticar o conhecimento da equipe sobre o assunto (item “a” do 4º passo). A partir daí, é fundamental divulgar efetivamente a importância do PBM, já que nem todos os profissionais de saúde diretamente envolvidos no cuidado ao paciente estão familiarizados ou engajados ativamente com ele. Portanto, para envolver toda a equipe é essencial o desenvolvimento de estratégias de comunicação que esclareçam os benefícios clínicos, cirúrgicos e operacionais do PBM usando dados científicos e exemplos práticos. Promover workshops, seminários e discussões interativas poderão ajudar a aumentar a conscientização e o engajamento, melhorando a adesão ao programa e garantindo seu sucesso, principalmente nas áreas-piloto envolvidas. O Grupo PBM-HU-UNIFESP já possui um sistema de treinamento que começou com a inclusão do PBM no curso de graduação em Medicina da EPM como uma disciplina eletiva, e um curso obrigatório de treinamento em PBM para todos os médicos residentes do HU/UNIFESP através da Comissão de Residência Médica (COREME). Recomenda-se que os cursos de treinamento incluam especialistas que abordem o PBM aplicado a várias áreas como: hematologia, anestesiologia, especialidades cirúrgicas, obstetrícia, pediatria, trauma e prática interprofissional. Por meio de parcerias ou convênios, esse curso pode ser oferecido a outros hospitais e instituições interessados.
Para o 6º passo a recomendação prática é que as ações possam ser planejadas com base nas condições de infraestrutura e pessoal identificadas pela avaliação local (item “b” do 4º passo). Como no exemplo do Grupo PBM-HU-UNIFESP, com base nos resultados da avaliação, devem ser listados os recursos locais disponíveis para diagnóstico e tratamento de anemias e coagulopatias, hemostáticos sistêmicos e tópicos, recuperação de células sanguíneas e testes viscoelásticos. Além disso, é importante verificar a disponibilidade de pessoal médico, de Enfermagem e técnico, residentes, e equipe administrativa que possam incorporar o PBM em suas rotinas e apoiar e se envolver na sua implementação. Inicialmente, não estão previstas contratações específicas para o PBM, considerando que sua implementação envolve muito mais a mudança de práticas e de mentalidade. A reorganização de rotinas e de pessoal se mostrou viável no exemplo do Grupo PBM-HU-UNIFESP. Através do diagnóstico local, um passo importante é desenvolver protocolos assistenciais baseados em evidências que incluam estratégias de PBM aplicáveis localmente e garantam a eficácia de sua implementação. Como exemplo do Grupo PBM-HU-UNIFESP, as ações são destacadas nos seguintes itens:
- a) Desenvolvimento de Protocolos: as recomendações para os protocolos assistenciais foram desenvolvidas após análise extensiva da literatura científica atual e intensas discussões entre os membros do Grupo de Trabalho e as áreas envolvidas, incluindo o Protocolo de Tratamento Farmacológico de Anemia e Diretrizes para Terapia com Eritropoetina (Figura 1) e o Protocolo de Manejo de Sangramento (Figura 2). As recomendações destes protocolos assistenciais para a prática clínica e cirúrgica são claras e objetivas e estão totalmente disponíveis para as instituições interessadas na implementação.
- b) Cuidados Pré-operatórios: a Disciplina de Hematologia e Hemoterapia e o Hemocentro da UNIFESP enfatizaram a importância da criação de um Ambulatório de Anemias do PBM. Este ambulatório pode ser criado a partir da reorganização dos serviços existentes nesses setores, inicialmente por um dia na semana, como feito no exemplo de implementação do PBM no HU/UNIFESP. Isso permite que pacientes ambulatoriais das áreas-piloto sejam preparados para os procedimentos cirúrgicos eletivos no tratamento das anemias e coagulopatias pré-operatórias com base nos princípios do PBM, através do Protocolo de Tratamento Farmacológico de Anemia e Diretrizes para Terapia com Eritropoetina (seção: pacientes cirúrgicos eletivos) acima mencionado. A mesma equipe de profissionais avalia pacientes hospitalizados em casos de cirurgias de urgência e emergência através de interconsultas, também seguindo as recomendações do Protocolo de Tratamento Farmacológico de Anemia e Diretrizes para Terapia com Eritropoetina (seção: pacientes cirúrgicos não eletivos), com tratamentos otimizados devido às restrições de tempo.
- c) Práticas Eficientes no Cuidado Intraoperatório: estabelecimento de práticas de manejo intraoperatório envolvendo as áreas de Anestesiologia e Cirurgia com base nos princípios do PBM, por meio do Protocolo de Manejo de Sangramento acima mencionado e da colaboração entre as equipes cirúrgica e de anestesiologia para otimizar o uso de hemostáticos sistêmicos e tópicos, recuperação de células sanguíneas e testes viscoelásticos.
- d) Práticas Eficientes no Cuidado Pós-operatório: reforço do conceito de tolerância à anemia entre os intensivistas responsáveis pelo cuidado pós-operatório na UTI, com base na condição individual do paciente. Aspectos importantes incluem nutrição precoce (oral/enteral/parenteral) para apoiar a eritropoese, evitar perdas sanguíneas iatrogênicas (coleta excessiva de sangue para exames laboratoriais) e tratar anemia e sangramentos. Nesse caso, os testes viscoelásticos também são relevantes para identificar as causas de possíveis sangramentos.
É necessário um investimento inicial para aquisição de novos medicamentos hemostáticos e para o tratamento de anemias, bem como para aquisição de equipamentos de recuperação de células sanguíneas e testes viscoelásticos que possam estar fora da rotina de alguns hospitais. No entanto, deve-se destacar que, ao reduzir o uso de hemocomponentes, os custos também serão significativamente reduzidos.


As recomendações para o 7º passo, de acordo com o exemplo do Grupo PBM-HU-UNIFESP, são definir uma data para a implementação do PBM, realizar um evento inaugural oficial para reforçar a importância do papel das equipes e do apoio pessoal, organizar as ações necessárias globalmente e estabelecer uma meta para compartilhar informações sobre a eficácia da implementação.
A recomendação para o 8º passo é manter as ações do Grupo de Trabalho, seguindo o exemplo do Grupo PBM-HU-UNIFESP. Na fase inicial será necessário monitoramento contínuo das ações, identificando dificuldades, ameaças ou resistências, considerando oportunidades e pontos fortes para superá-las e permitindo que o processo progrida de forma eficaz. Reuniões quinzenais podem ser suficientes. Essa tarefa de gestão do PBM também inclui analisar o acréscimo e o momento adequado para integração de novas áreas e setores hospitalares no processo de implementação. No caso do Grupo PBM-HU-UNIFESP, os gestores incorporaram o PBM como um projeto institucional para melhorar a linha de cuidado do paciente em vários processos hospitalares visando reduzir morbidades, mortalidade e os custos.
A recomendação para o 9º passo é a necessidade de sistematizar a aquisição de dados relacionados à implementação para avaliação técnica, gerenciada pelo Grupo de Trabalho. Para garantir o sucesso da implementação do PBM é essencial utilizar sistemas informatizados e adotar a coleta sistemática de dados dos pacientes submetidos ao protocolo. Esses sistemas facilitam a análise dos resultados e o monitoramento do impacto do PBM ao longo do tempo. A avaliação anual dos resultados é fundamental, com a definição de indicadores de desempenho, análises estatísticas e o envolvimento de todas as partes interessadas. Esse processo identifica campos para melhoria contínua e promove a excelência na linha de cuidado do paciente através do PBM. Além disso, a implementação de um sistema de monitoramento e avaliação mede a adesão aos protocolos de PBM e seus impactos, permitindo ajustes oportunos e melhorias contínuas. Essas medidas promovem um ambiente colaborativo e estruturado que melhora a adesão ao PBM e os resultados clínicos. A aquisição de dados deve focar em índices diretamente impactados pela implementação do PBM, conforme evidenciado na literatura[3,4,8]. Os índices relacionados à segurança do paciente incluem: o uso de hemocomponentes (tipo e número de unidades), taxas de infecção, tempo de internação, reoperações, acidentes vasculares, complicações pós-operatórias e mortalidade, conforme recomendado pelo Grupo PBM-HU-UNIFESP. Esses índices podem quantificar a economia de recursos através da redução do uso de hemocomponentes, menor tempo de internação e menos complicações.
A recomendação para o 10º passo é que as ações de auditoria e conformidade da implementação sejam conduzidas por um comitê consultivo vinculado à diretoria clínica, dada sua natureza de controle institucional. Recomenda-se que este comitê inclua pelo menos dois médicos membros do Grupo de Trabalho, um representante do setor de garantia de qualidade ou de segurança do paciente, um representante da gerência administrativa e um representante da Enfermagem. Este comitê desempenha um papel burocrático na organização de informações, análise de desempenho, avaliação de resultados e apoio à gestão hospitalar.
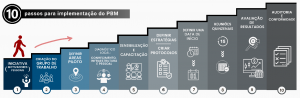
Todos os passos para a implementação do PBM estão ilustrados na Figura 3.
DISCUSSÃO
Recomendação Baseada em Evidências
A implementação bem-sucedida do programa PBM depende fortemente da intensa mobilização dos envolvidos, principalmente no âmbito do Grupo de Trabalho, que deve motivar outras partes interessadas das áreas-piloto bem como gestores, residentes e equipe administrativa. Isso porque, como exemplificado pelo Grupo PBM-HU-UNIFESP, o processo de implementação começa de forma idealista, impulsionado pelo compromisso de todos em melhorar a segurança do paciente e alocar recursos públicos de maneira eficiente. Neste exemplo, todas as ações foram realizadas sem quaisquer conflitos de interesse, nem com fabricantes de produtos ou equipamentos, nem com instituições fornecedoras de hemocomponentes. O processo de implementação do PBM levou a uma reavaliação da linha de cuidado do paciente resultando em melhorias na preparação pré-operatória, otimização das práticas cirúrgicas e critérios mais rigorosos para o uso de hemocomponentes. No cenário de um hospital universitário, houve notável envolvimento científico das especialidades médicas e de Enfermagem, motivando a participação de programas de pós-graduação e pesquisa institucionais existentes e motivando ainda mais os residentes. Essas ações também facilitaram a criação de um espaço de integração entre diferentes áreas, promovendo um ambiente de troca de conhecimento e melhores práticas. Assim, com base nessas recomendações que incluem um relato de experiência de implementação (Grupo PBM-HU-UNIFESP), a importância da motivação entre todas as partes interessadas torna-se evidente. Como resultado, é estratégico envolver não apenas os gestores, mas toda a equipe de saúde. Nesse sentido, além do desenvolvimento de fluxos e processos, o envolvimento direto dos profissionais de saúde da linha de frente é a chave para o sucesso. Acima de tudo, a educação se destaca como o fator principal pois o conhecimento muda comportamento.
De fato, um estudo recente[13] procurou analisar as motivações por trás das prescrições de concentrado de hemácias por anestesiologistas e cirurgiões, uma vez que essas motivações conduzem à tomada de decisões e podem explicar a variabilidade significativa dessa prática entre médicos e hospitais. Vários aspectos foram identificados, incluindo: (1) conhecimento, (2) papel e identidade social/profissional, (3) crenças sobre as consequências, (4) recursos e contexto ambiental, (5) influências sociais, (6) regulação comportamental, (7) natureza dos comportamentos e (8) processos de memória, atenção e decisão. Pode-se observar como os esforços educacionais e motivacionais dos envolvidos na implementação do PBM são mais importantes do que meras decisões administrativas, dada a grande variedade de fatores que influenciam essas decisões clínicas. Portanto, os aspectos educacionais devem ser considerados tão relevantes quanto a necessidade de fluxos e processos administrativos.
A recomendação do protocolo citado e utilizado pelo Grupo PBM-HU-UNIFESP para o Tratamento Farmacológico de Anemia e Diretrizes para Terapia com Eritropoetina contém estratégias para vários cenários, considerando as principais causas de anemia, pacientes cirúrgicos (eletivos e não eletivos) e não cirúrgicos, formas otimizadas de reposição de ferro, uso de eritropoetina (EPO) e precauções necessárias no uso desses medicamentos. De fato, o tratamento das anemias desempenha um papel central na implementação do PBM. O estudo de Warner et al.[14] em cirurgia cardíaca demonstrou a associação entre anemia pré-operatória e piores desfechos, incluindo lesão renal aguda e aumento do tempo de internação. As lesões orgânicas perioperatórias causadas por isquemia tecidual decorrente da anemia induzem a inflamação secundária e a elevações de citocinas pró-inflamatórias, que podem ser exacerbadas pelo dano inflamatório da circulação extracorpórea. Além disso, a anemia pré-operatória é um fator de risco significativo para transfusão perioperatória de concentrado de hemácias, que por sua vez está associada a desfechos clínicos adversos. Nesse contexto, uma atualização recente da Society for the Advancement of Patient Blood Management [15] (Sociedade para o Avanço do Gerenciamento do Sangue do Paciente) enfatizou o papel significativo da EPO (juntamente com o ferro) no tratamento de anemias para pacientes eletivos, tornando-se um recurso valioso quando há tempo limitado para a preparação de cirurgias não eletivas. O documento indica que os potenciais riscos de eventos cardiovasculares associados à EPO não ocorrem e ela pode até ter um efeito nefroprotetor. Além disso, na cirurgia cardíaca, ocorrem os seguintes eventos: os betabloqueadores suprimem a produção endógena de EPO, e a anemia perioperatória diminui o efeito cardioprotetor dos betabloqueadores; citocinas estimuladas pela resposta inflamatória associada à circulação extracorpórea limitam a produção de EPO; e a isquemia renal perioperatória pode limitar a produção de EPO. Portanto, o uso de EPO alguns dias antes da cirurgia cardíaca torna-se relevante para a redução do volume de concentrado de hemácias. Além disso, o uso de EPO pode reduzir significativamente a probabilidade de uso de concentrado de hemácias no perioperatório (de 93% para 67%) e uma única dose de 80.000 UI de EPO dois dias antes da cirurgia reduziu o uso pós-operatório de concentrado de hemácias em 22%. Consequentemente, estudos mostram diminuição de custos com o tratamento pré-operatório da anemia por reduzir o uso de concentrado de hemácias e as complicações perioperatórias associadas[1,8,9].
A recomendação do Protocolo de Manejo de Sangramento mencionado acima, utilizado pelo Grupo PBM-HU-UNIFESP, contém as melhores diretrizes e prescrições de hemostáticos sistêmicos em vários cenários clínico-cirúrgicos, opções e recomendações para hemostáticos tópicos, o uso de dispositivos de recuperação de células sanguíneas e hemodiluição normovolêmica aguda. O uso de agentes antifibrinolíticos sintéticos, como ácido tranexâmico ou ácido epsilon-aminocaproico, reduz a perda de sangue e a necessidade de transfusão sanguínea durante procedimentos cardíacos, traumas, sangramento menstrual intenso, hemorragia periparto, lesão cerebral traumática e sangramento no local cirúrgico[15]. De fato, seu uso otimizado, dentro da lógica do PBM descrita no protocolo, é um poderoso aliado no controle de sangramentos e evita o uso de transfusões de sangue alogênico. Outro elemento importante para conservar o sangue do próprio paciente é o uso da recuperação de células sanguíneas. Um artigo de revisão de Ashworth & Klein[16] analisou o uso de recuperação de células sanguíneas, seus benefícios, riscos e possíveis complicações em vários cenários como cirurgia cardíaca e vascular, neurocirurgia, obstetrícia, ortopedia, pediatria e oncologia. Conforme relatado na revisão, a recuperação de células sanguíneas é segura e eficaz na redução de transfusões de sangue em cirurgias eletivas de adultos nas áreas analisadas, particularmente em cirurgias cardíacas e ortopédicas. Seu uso deve ser considerado em casos em que se espera uma perda sanguínea significativa (500 mL)[17]. Em casos de malignidade, seu uso com um filtro de depleção de leucócitos (FDL) parece seguro. Em pacientes obstétricas, o uso de FDLs não é recomendado. Estudos adicionais são necessários para a sua consolidação em ambos os casos. A única contraindicação absoluta para o uso da recuperação de células sanguíneas é a recusa do paciente. Essa revisão também destaca a relação custo-efetividade do uso de recuperação de células sanguíneas em comparação com a transfusão de sangue alogênico. Seu uso demonstrou ser custo-efetivo (com ênfase em cirurgias cardíacas e ortopédicas) e dados já demonstraram uma economia de U$ 110,54 dólares com o uso da recuperação de células sanguíneas em comparação com a transfusão de uma unidade de sangue alogênico[16]. Nesse contexto de custo-efetividade, a hemodiluição normovolêmica aguda é uma técnica intraoperatória de baixo custo para conservar o sangue do próprio paciente. Ela é realizada imediatamente antes do procedimento cirúrgico e envolve a remoção do sangue total do paciente em bolsas de sangue vazias, calculadas individualmente, enquanto se mantém o volume do paciente com soluções cristaloides e/ou coloides. O sangue removido é devolvido ao paciente imediatamente após o procedimento cirúrgico. A hemodiluição normovolêmica aguda tem sido realizada com sucesso em cirurgias cardíacas desde a década de 1970. Atualmente, vários estudos têm mostrado que ela é segura, de baixo custo e eficaz na redução da necessidade de transfusões sanguíneas em cirurgias abdominais[18].
Em relação à mudança no conceito de tolerância à anemia, uma revisão recente levanta uma questão importante em seu título: “Gatilhos para Transfusão de Hemácias: Há Algo Novo?”[19]. Essa revisão destaca que, por muitos anos, a regra tradicional 10/30 (hemoglobina 10 g/dL, hematócrito 30%) tem sido usada como gatilho para transfusões de sangue alogênico. Acredita-se agora que esse conceito tenha contribuído para inúmeras transfusões desnecessárias e para um número desconhecido de mortes relacionadas a múltiplas transfusões. Como destacado pelos autores, estudos recentes mostram que níveis mais baixos de hemoglobina podem ser aceitos com segurança, mesmo em pacientes criticamente enfermos. Além disso, esses novos limiares para transfusão restritiva estão muito além dos limites teóricos de tolerância individual à anemia. Embora esse conceito possa parecer intuitivo à primeira vista, os autores demonstraram que não há evidências científicas sólidas que apoiem a segurança e o benefício de confiar apenas em gatilhos laboratoriais para prescrever transfusões de sangue alogênico. Nesse sentido, essa publicação nos incentiva a continuar buscando parâmetros mais sensíveis e específicos em relação às condições clínico-cirúrgicas gerais de cada paciente, pois estudos envolvendo pacientes que recusam transfusões de sangue mostram que o organismo de fato tolera a anemia mais do que os próprios médicos.
Áreas como transplante de fígado, agora incluídas no processo de implementação do Grupo PBM-HU-UNIFESP, também se beneficiaram dos princípios do PBM. Uma publicação recente[20] mostrou que as transfusões de sangue alogênico no transplante de fígado aumentam significativamente a morbidade e mortalidade pós-transplante e estão associadas à redução da sobrevida do enxerto. Nesse contexto, o PBM surge como uma alternativa importante. Na Medicina Intensiva, também incluída no exemplo do Grupo PBM-HU-UNIFESP apresentado aqui, os pacientes apresentam múltiplos fatores de risco para anemia e comorbidades e o PBM oferece estratégias individualizadas que contribuem significativamente para o manejo da anemia, coagulopatias e perda sanguínea iatrogênica[21]. Na população pediátrica, uma revisão recente destaca a relevância significativa de se desenvolver programas de PBM para neonatos e crianças e os desafios a esse respeito, demonstrando que não devem ser usados os mesmos conceitos e parâmetros dos programas de PBM empregados para adultos. No entanto, é urgente que essa área seja incluída o mais rápido possível na estratégia de PBM[22].
Como mensagem final, o PBM traz melhores resultados para as equipes de saúde, pacientes e populações vulneráveis com deficiências de micronutrientes, anemia e/ou sangramento. Ele também traz benefícios financeiros significativos para hospitais públicos e privados e sistemas de saúde. A Organização Mundial da Saúde (OMS) declarou urgência na implementação do PBM em seus 194 países membros devido à segurança do paciente, aos altos custos das transfusões de sangue, ao envelhecimento da população e às potenciais novas pandemias. Segundo Hofmann et al.[5], a implementação do PBM envolve os chamados 3Es — Evidência, Economia e Ética — que justificam plenamente a urgência de sua implementação.
Limitações
Como limitações, os resultados econômicos do exemplo de implementação apresentado aqui não foram incluídos, o que será feito em publicações futuras.
CONCLUSÃO
As evidências científicas atuais apoiam a eficácia do PBM em reduzir a necessidade de transfusões de sangue, diminuir as complicações associadas e a mortalidade, e promovendo um PBM mais eficiente e seguro. Assim, o PBM não só melhora os resultados clínicos para os pacientes, mas também contribui para a sustentabilidade econômica dos sistemas de saúde. A implementação deste programa pode levar a práticas médicas otimizadas, trazendo benefícios tanto para os pacientes quanto para os sistemas de saúde. Portanto, com base nas evidências atuais, a implementação e disseminação do PBM em hospitais e centros de saúde é fortemente recomendada. O objetivo desta revisão foi resumir as estratégias do PBM em uma abordagem abrangente e baseada em evidências através de um modelo sistemático e estruturado para a implementação do PBM em hospitais terciários. As recomendações propostas aqui são de pesquisadores e especialistas de um hospital universitário de alta complexidade da rede SUS, apresentando-se como uma estratégia que pode ser seguida como diretriz para a implementação do PBM em outros contextos.
AGRADECIMENTOS
Aos gestores da Associação Paulista para o Desenvolvimento da Medicina (SPDM) que, como gestores do HU/UNIFESP, apoiaram esta proposta desde o início. Aos diretores clínico e técnico do HU/UNIFESP. Aos membros universitários da EPM/UNIFESP envolvidos na implementação do PBM, no ensino do PBM e no grupo de pesquisa Estudos Avançados em Gerenciamento de Sangue do Paciente (Programa de Pós-Graduação em Medicina: Hematologia e Oncologia). Aos setores de Suprimentos, Farmácia, Compras e Engenharia Clínica do HU/UNIFESP. A todos os profissionais de saúde e a todos os envolvidos e engajados no desenvolvimento das recomendações e na implementação do PBM no HU/UNIFESP. Seu comprometimento, dedicação e colaboração foram essenciais no desenvolvimento das recomendações e na implementação do PBM. Visite nosso site: https://pbm.unifesp.br.
Apoio financeiro: Fundação de Amparo à Pesquisa do Estado de São Paulo (FAPESP) (processo 2022/15920-7) e CAPES PrInt UNIFESP (processo 88887.310780/2018-00).
Sem conflito de interesse.
Papéis e Responsabilidades dos Autores
ICC – Contribuições substanciais para a concepção ou elaboração do trabalho; ou aquisição, análise ou interpretação dos dados para o trabalho; redação do trabalho ou revisão crítica para conteúdo intelectual importante; concordância em ser responsável por todos os aspectos do trabalho, garantindo que questões relacionadas à exatidão ou integridade de qualquer parte do trabalho sejam devidamente investigadas e resolvidas; aprovação final da versão a ser publicada.
MSF – Contribuições substanciais para a concepção ou elaboração do trabalho; ou aquisição, análise ou interpretação dos dados para o trabalho; redação do trabalho ou revisão crítica para conteúdo intelectual importante; aprovação final da versão a ser publicada.
NAHJ – Contribuições substanciais para a concepção ou elaboração do trabalho; ou aquisição, análise ou interpretação dos dados para o trabalho; redação do trabalho ou revisão crítica para conteúdo intelectual importante; aprovação final da versão a ser publicada.
ICS – Contribuições substanciais para a concepção ou elaboração do trabalho; ou aquisição, análise ou interpretação dos dados para o trabalho; redação do trabalho ou revisão crítica para conteúdo intelectual importante; aprovação final da versão a ser publicada.
RCR – Contribuições substanciais para a concepção ou elaboração do trabalho; ou aquisição, análise ou interpretação dos dados para o trabalho; redação do trabalho ou revisão crítica para conteúdo intelectual importante; aprovação final da versão a ser publicada.
MMOB – Redação do trabalho ou revisão crítica para conteúdo intelectual importante; aprovação final da versão a ser publicada.
MAPN – Contribuições substanciais para a concepção ou elaboração do trabalho; ou aquisição, análise ou interpretação dos dados para o trabalho; redação do trabalho ou revisão crítica para conteúdo intelectual importante; aprovação final da versão a ser publicada.
FCA – Redação do trabalho ou revisão crítica para conteúdo intelectual importante; aprovação final da versão a ser publicada.
BBB – Aprovação final da versão a ser publicada.
AMG – Aprovação final da versão a ser publicada.
FVCS – Contribuições substanciais para a concepção ou elaboração do trabalho; ou aquisição, análise ou interpretação dos dados para o trabalho; aprovação final da versão a ser publicada.
NBJ – Contribuições substanciais para a concepção ou elaboração do trabalho; ou aquisição, análise ou interpretação dos dados para o trabalho; aprovação final da versão a ser publicada.
IAC – Aprovação final da versão a ser publicada.
CMMS – Aprovação final da versão a ser publicada.
CSMM – Aprovação final da versão a ser publicada.
LS – Aprovação final da versão a ser publicada.
VP – Aprovação final da versão a ser publicada.
SLA – Aprovação final da versão a ser publicada.
LSPR – Aprovação final da versão a ser publicada.
SG – Redação do trabalho ou revisão crítica para conteúdo intelectual importante; aprovação final da versão a ser publicada.
ISR – Redação do trabalho ou revisão crítica para conteúdo intelectual importante; aprovação final da versão a ser publicada.
NSM – Contribuições substanciais para a concepção ou elaboração do trabalho; ou aquisição, análise ou interpretação dos dados para o trabalho; aprovação final da versão a ser publicada.
JSOA – Redação do trabalho ou revisão crítica para conteúdo intelectual importante; aprovação final da versão a ser publicada.
AAS – Contribuições substanciais para a concepção ou elaboração do trabalho; ou aquisição, análise ou interpretação dos dados para o trabalho; redação do trabalho ou revisão crítica para conteúdo intelectual importante; aprovação final da versão a ser publicada.
CEP – Contribuições substanciais para a concepção ou elaboração do trabalho; ou aquisição, análise ou interpretação dos dados para o trabalho; redação do trabalho ou revisão crítica para conteúdo intelectual importante; concordância em serem responsáveis por todos os aspectos do trabalho, garantindo que questões relacionadas à exatidão ou integridade de qualquer parte do trabalho sejam devidamente investigadas e resolvidas; aprovação final da versão a ser publicada.
REFERÊNCIAS
- Anthes E. Evidence-based medicine: Save blood, save lives. Nature. 2015 Apr 2;520(7545):24–6.
- Vargas, L.D., Garcia, L.O., Galvão, A., Onsten, T.G., Coitinho, A.S., & Sekine, L.. Blood transfusion-related immunomodulation. Clinical & Biomedical Research. 2014;34:333-341.
- Farmer 2013, Marik PE, Corwin HL. Efficacy of red blood cell transfusion in the critically ill: a systematic review of the literature. Crit Care Med. 2008 Sep;36(9):2667-74.
- Farmer SL, Towler SC, Leahy MF, Hofmann A. Drivers for change: Western Australia Patient Blood Management Program (WA PBMP), World Health Assembly (WHA) and Advisory Committee on Blood Safety and Availability (ACBSA). Best Pract Res Clin Anaesthesiol. 2013 Mar;27(1):43–58.
- Hofmann A, Shander A, Blumberg N, Hamdorf JM, Isbister JP, Gross I. Patient Blood Management: Improving Outcomes for Millions While Saving Billions. What Is Holding It Up? Anesth Analg. 2022 Sep 1;135(3):511-523.
- Jadwin DF, Fenderson PG, Friedman MT, Jenkins I, Shander A, Waters JH, et al. Determination of Unnecessary Blood Transfusion by Comprehensive 15-Hospital Record Review. The Joint Commission Journal on Quality and Patient Safety. 2023 Jan;49(1):42–52.
- Santos AA, Silva JP, Silva Lda F, Sousa AG, Piotto RF, Baumgratz JF. Therapeutic options to minimize allogeneic blood transfusions and their adverse effects in cardiac surgery: a systematic review. Rev Bras Cir Cardiovasc. 2014 Oct-Dec;29(4):606-21.
- World Health Organization. (2021). The urgent need to implement patient blood management: policy brief. World Health Organization. https://apps.who.int/iris/handle/10665/346655. Licença: CC BY-NC-SA 3.0 IGO.
- Pavenski K, Howell A, Mazer CD, Hare GMT, Freedman J. ONTraC: A 20-Year History of a Successfully Coordinated Provincewide Patient Blood Management Program: Lessons Learned and Goals Achieved. Anesth Analg. 2022 Sep 1;135(3):448-458.
- Brasil. Ministério da Saúde. Secretaria de Assistência à Saúde. Manual Brasileiro de Acreditação Hospitalar / Secretaria de Assistência à Saúde. – 3. ed. rev. e atual. – Brasília: Ministério da Saúde, 2002.
- Vaena MM de V, Alves LA. Assessment of the knowledge and perceptions of Brazilian medical residents on transfusion medicine. Hematol Transfus Cell Ther. 2019;41(1).
- Al-Riyami AZ, Louw VJ, Indrikovs AJ, Nedelcu E, Bakhtary S, Eichbaum QG, Smit Sibinga CT; Education Subcommittee of the AABB Global Transfusion Forum. Global survey of transfusion medicine curricula in medical schools: Challenges and opportunities. Transfusion. 2021 Feb;61(2):617-626.
- Lenet T, Tropiano J, Skanes S, Ivankovic V, Verret M, McIsaac DI, Tinmouth A, Nicholls SG, Patey AM, Fergusson DA, Martel G. Understanding Intraoperative Transfusion Decision-Making Variability: A Qualitative Study. Transfus Med Rev. 2023 Apr;37(2):150726.
- Warner MA, Hanson AC, Schulte PJ, Sanz JR, Smith MM, Kauss ML, Crestanello JA, Kor DJ. Preoperative Anemia and Postoperative Outcomes in Cardiac Surgery: A Mediation Analysis Evaluating Intraoperative Transfusion Exposures. Anesth Analg. 2024 Apr 1;138(4):728-737.
- Tibi P, McClure RS, Huang J, Baker RA, Fitzgerald D, Mazer CD, Stone M, Chu D, Stammers AH, Dickinson T, Shore-Lesserson L, Ferraris V, Firestone S, Kissoon K, Moffatt-Bruce S. STS/SCA/AmSECT/SABM Update to the Clinical Practice Guidelines on Patient Blood Management. J Extra Corpor Technol. 2021 Jun;53(2):97-124.
- Ashworth A, Klein AA. Cell salvage as part of a blood conservation strategy in anaesthesia. Br J Anaesth. 2010 Oct;105(4):401-16.
- Klein AA, Bailey CR, Charlton AJ, Evans E, Guckian-Fisher M, McCrossan R, Nimmo AF, Payne S, Shreeve K, Smith J, Torella F. Association of Anaesthetists guidelines: cell salvage for peri-operative blood conservation 2018. Anaesthesia. 2018 Sep;73(9):1141-1150.
- Wakiya T, Ishido K, Kimura N, Nagase H, Kanda T, Kubota S, Fujita H, Takahashi Y, Yamamoto T, Chida K, Saito J, Hirota K, Hakamada K. Postoperative long‑term outcomes of acute normovolemic hemodilution in pancreatic cancer: A propensity score matching analysis. Oncol Lett. 2024 Mar 27;27(5):236.
- Tomic Mahecic T, Dünser M, Meier J. RBC Transfusion Triggers: Is There Anything New? Transfus Med Hemother. 2020 Oct;47(5):361-368.
- Pérez-Calatayud AA, Hofmann A, Pérez-Ferrer A, Escorza-Molina C, Torres-Pérez B, Zaccarias-Ezzat JR, Sanchez-Cedillo A, Manuel Paez-Zayas V, Carrillo-Esper R, Görlinger K. Patient Blood Management in Liver Transplant-A Concise Review. Biomedicines. 2023 Apr 4;11(4):1093.
- Hof L, Choorapoikayil S, Meybohm P, Zacharowski K. Patient Blood Management in intensive care patients. Curr Opin Crit Care. 2021 Dec 1;27(6):709-716.
- Goel R, Cushing MM, Tobian AA. Pediatric Patient Blood Management Programs: Not Just Transfusing Little Adults. Transfus Med Rev. 2016 Oct;30(4):235-41.