A cirurgia cardiovascular certamente é um dos instrumentos mais poderosos da medicina para modificar desfechos e melhorar a sobrevida de pacientes que possuem doenças graves, debilitantes e capazes de levar ao óbito. Contudo, em decorrência do acesso cirúrgico, da circulação extracorpórea, do clampeamento e da manipulação vascular, o procedimento traz consigo riscos de morbidade e mortalidade inerentes que devem sempre ser considerados.
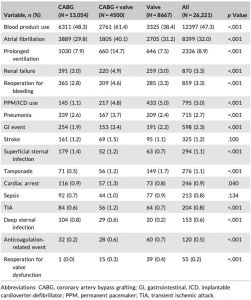
Nas cirurgias mais comuns, como revascularização do miocárdio, cirurgias de valvopatias ou combinações das duas, encontramos na literatura (Tabela 1) um risco de 47,3% de necessidade de hemotransfusão, 32,0% de fibrilação atrial, 8,9% de ventilação mecânica prolongada, 3,3% de lesão renal aguda e necessidade de reoperação por sangramento e 3,0% de necessidade de implante de marca-passo ou cardiodesfibrilador.1
Em busca de reduzir complicações, certamente o primeiro passo deve ser conhecer a taxa de complicações do serviço ou do cirurgião. Experiências prévias, como a do Instituto do Coração do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo (InCor-HCFMUSP), mostraram que o estabelecimento de metas e métricas, a apresentação pública e mensal dos resultados e a monitorização da aderência a protocolos perioperatórios por um programa de qualidade foram capazes, por si só, de reduzir a mortalidade global do serviço de 7,8 para 5%, em coronária de 5,8 para 3,1%, em cirurgias valvares de 14% para 7,5 e em cardiopatias congênitas de 12,1 para 9,6%.2
Ao analisar os resultados, percebe-se que a melhora ocorreu sem qualquer mudança padronizada na técnica cirúrgica e foi observada apesar dos pacientes atendidos serem cada vez mais comórbidos e passarem por procedimentos mais complexos.3 Filosoficamente, pode-se inferir que uma parcela da mudança pode ter ocorrido pela mudança de comportamento dos indivíduos que tende a ocorrer pelo simples fato de estarem sendo observados: o efeito Hawthorne.4
Esse efeito foi descrito a partir das observações da produtividade da fábrica Western Electric Company, no bairro de Hawthorne, em Chicago. Entre 1924 e 1927, foi conduzido o Illumination Experiment, em que alterações mínimas na iluminação, que implicavam o quanto os trabalhadores eram observados pelos supervisores, modificavam seu nível de produtividade, positiva ou negativamente.

Fonte: https://www.assemblymag.com/articles/88188-the-hawthorne-works
Contudo, seria muito reducionista atribuir a mudança nos resultados apenas a esse efeito em uma cirurgia tão complexa como a cardiovascular. Na verdade, a observação atenta na coleta, análise e apresentação dos dados pode permitir que cada serviço ou cirurgião identifique os pontos de fragilidade na jornada perioperatória do paciente e busque formas de melhorar seus desfechos.
Pode-se, ainda, otimizar os esforços se conseguirmos refinar suficientemente os dados para cada desfecho (p. ex., infecção, lesão renal aguda, fibrilação atrial pós-operatória) e iniciar protocolos assistenciais que incluam medidas que objetivem melhorar os resultados de cada um deles.
Uma iniciativa interessante que busca unir estratégias baseadas em evidências para otimizar a recuperação do paciente e prevenir complicações é o Enhanced Recovery After Cardiac Surgery (ERACS). Publicado em 2024, juntamente com a Society of Thoracic Surgery (STS), seu consenso conjunto para o cuidado perioperatório em cirurgia cardíaca organizou as medidas em fases (pré, intra e pós-operatório) e em pacotes (bundles) de estratégias multifases que visam otimizar um desfecho específico.5
A seguir, serão brevemente discutidas estratégias de cada ponto da jornada perioperatória que possuem evidências de implicar redução de complicações pós-operatórias, seguindo a ordem de apresentação do consenso supracitado.
1. Avaliação do risco pré-operatório
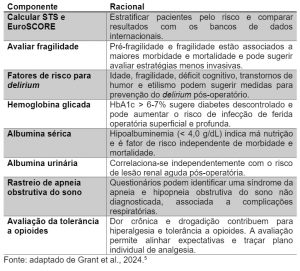
Estimar o risco de morbidade e mortalidade do paciente é um dos meios para identificar pontos para otimizar clinicamente o paciente para a cirurgia ou lançar meio de estratégias preemptivas (Tabela 2).
2. Pré-habilitação
Para otimizar pacientes com fragilidade e/ou desnutrição, a pré-habilitação pode reduzir complicações pós-operatórias (OR 0,41, IC 95% 0,28-0,62), reduzir o tempo de internação (SMD = −0,56 dias, IC 95% −1,13-−0,01) e melhorar a função pulmonar em termos da pressão inspiratória máxima (SMD = 0,66, IC 95% 0,35-0,96).6 A pré-habilitação consiste em um plano individualizado e que pode ser organizado pelo acrônimo NEW: Nutrition, Exercise and Worry. Arora et al. sugeriram medidas nestas três frentes: 1) modificar dieta para combater a desnutrição proteica; 2) plano individualizado de exercícios para melhorar a capacidade funcional basal, quando factível; 3) medidas para aliviar a ansiedade e o estresse pré-operatórios.7
3. Abreviação do jejum
Já é amplamente aceito por consensos das Sociedades de Anestesiologia americana e europeia que o jejum de 2 horas para líquidos claros sem resíduos e de 6 a 8 horas para sólidos é seguro antes de uma cirurgia eletiva, excetuando-se os pacientes com fração de ejeção reduzida, esvaziamento gástrico retardado e uso frequente de ecocardiograma transtorácico.8,9 Costumeiramente, a abreviação é feita com 200 a 500 mL de maltodextrina ou com Gatorade®, por exemplo.
Essa medida pode reduzir o nível de cortisol pré-operatório, afetando a resistência à insulina, e o risco de broncoaspiração pode ser reduzido ao verificar o esvaziamento gástrico utilizando a ultrassonografia pré-indução anestésica.10
4. Ecocardiograma transesofágico intraoperatório
Essencial à avaliação minuciosa das cardiopatias estruturais, formação de trombos e anomalias congênitas, o ecocardiograma transesofágico intraoperatório (ETE) já é bem estabelecido nas cirurgias valvares e congênitas, reduzindo o risco de acidente vascular cerebral (pelo auxílio na retirada de ar das câmaras), reoperação (confirma a efetividade do procedimento) e mortalidade em 30 dias.11 Contudo, na revascularização de pacientes com médio a alto risco cardiovascular (STS > 4%), grandes registros já evidenciaram que houve uma redução de mortalidade, ao auxiliar na avaliação valvar, no diagnóstico de disfunções segmentares ou globais e na avaliação da etiologia do comprometimento hemodinâmico.12
5. Ventilação mecânica protetora
Para combater uma incidência de até 25% de complicações pulmonares no pós-operatório, medidas como volume corrente baixo (6-8 mL/kg), manutenção de pressão expiratória final positiva (PEEP) ≥ 5 cmH2O, baixa driving pressure (Ppico – PEEP ≤ 16 cmH2O) e manobras de recrutamento alveolar reduzem o risco de disfunção e complicações pulmonares.13,14
Durante a circulação extracorpórea, a cessação completa da ventilação induz uma atelectasia praticamente total dos pulmões, melhorando a exposição cirúrgica. Contudo, essa medida implica um aumento da atividade de leucócitos e ativa maior atividade inflamatória. Com isso, evidências moderadas sugerem que manter uma ventilação com PEEP mínima, ventilação em baixo volume corrente e baixa frequência pode reduzir a atelectasia sem atrapalhar a exposição cirúrgica, implicando melhora das trocas gasosas e redução de complicações pulmonares no pós-operatório.15
6. Monitorização do sistema nervoso central
Métodos de monitorização do sistema nervoso central (SNC), como o monitor de índice bispectral (BIS) ou espectroscopia próxima ao infravermelho (NIRS), foram desenvolvidos para identificar períodos de má perfusão cerebral e permitir a adequada titulação de anestésicos. Ainda não está claro qual o tipo de intervenção mais adequada a partir do diagnóstico de uma pior perfusão cerebral (hemotransfusão, oxigênio suplementar, titulação de vasopressores), mas estudos com o uso de NIRS foram associados à prevenção de déficits cognitivos no pós-operatório.16
7. Prevenção de náuseas e vômitos pós-operatórios
Considerando uma ampla e variável incidência de 10 a 70% de náuseas e vômitos pós-operatórios (PONV) na cirurgia cardíaca, sugere-se que avaliem fatores de risco para tal:
- a) Sexo feminino.
- b) Não tabagistas.
- c) História de PONV ou vertigem.
- d) Uso de opioides no pós-operatório.
Com base no número de fatores de risco já mencionados, sugere-se associar tal quantidade de classes de antieméticos de forma multimodal, podendo incluir:
1) Inibidores do 5HT-3 (p. ex., ondansetrona).
2) Corticosteroides (p. ex., dexametasona).
3) Antidopaminérgicos (p. ex., haloperidol, metoclopramida).
4) Anti-histamínicos.
5) Antagonistas do receptor NK1 (p. ex., aprepitanto).
6) Gabapentinoides (p. ex., pregabalina).
São reconhecidas ainda algumas medidas não farmacológicas, como hidratação, a própria abreviação de jejum, oxigênio suplementar, uso de gomas de mascar, gengibre e aromaterapia.17
8. Perfusão guiada por metas
A perfusão guiada por metas é uma forma mais sofisticada e completa de analisar se o paciente está recebendo fluxo sanguíneo adequado para o corpo durante a perfusão. Em vez de se basear apenas em um índice cardíaco e um hematócrito mínimos, utiliza-se o cálculo de entrega de oxigênio (DO2), que deve estar acima de 280 mL/min.m2 no paciente em hipotermia leve (32-34 °C), reduzindo o risco de lesão renal aguda estágio 1, o tempo de ventilação e o composto dos desfechos de morbidade e mortalidade do escore do STS.18
9. Estratégias para extubação precoce
Há evidências de que a extubação precoce após cirurgias eletivas, realizada até 6 horas da chegada à Unidade de Terapia Intensiva, inclusive durante a noite (se há equipe para supervisão adequada), é segura e reduz o tempo de internação hospitalar, acelerando a recuperação.19,20 Pode-se assegurar a segurança e tempos cada vez menores até a extubação ao se estabelecerem protocolos predeterminados.
Tais protocolos investigam estabilidade hemodinâmica, ação residual do bloqueio neuromuscular, capacidade ventilatória espontânea do paciente e outros fatores de risco, para garantir uma extubação com mínima chance de eventos adversos. Os pacientes de maior risco cirúrgico apresentam o maior benefício com o estabelecimento de protocolos bem definidos, com redução de 9,2 horas para 5,7 horas (p < 0,0001), enquanto os pacientes no geral reduzem de 7,4 horas para as mesmas 5,7 horas.19
Alguns estudos mostraram que a extubação em sala pode ser segura, com taxas de complicação e reintubação semelhantes às dos protocolos de extubação tradicionais, e efetiva por reduzir tempo de UTI, internação hospitalar e 20% dos custos hospitalares totais.21 Contudo, deve-se analisar cuidadosamente os pacientes elegíveis para extubação em sala, considerando o risco de sangramento pós-operatório, acidose e despertar tardio. Os estudos evitaram essa estratégia em pacientes submetidos a reoperações ou a cirurgias de maior tempo operatório, portadores de doença renal crônica ou diabetes e após a necessidade de inserção de balão intra-aórtico.22
10. Prevenção de lesão renal aguda
Pela alta incidência (de 20 a 40%) de lesão renal aguda após cirurgia cardíaca e pelo fato de que ela aumenta o risco de doença renal crônica e mortalidade a curto e longo prazo, devemos nos atentar aos pacientes com maior risco ou que estabeleceram a lesão no pós-operatório. O consenso da Kidney Disease: Improving Global Outcomes (KDIGO) sugere realizar monitorização seriada da creatinina sérica, quantificação rígida da diurese, reposição volêmica adequada, manutenção de alvos hemodinâmicos e evitar agentes nefrotóxicos.23
11. Medidas a serem realizadas por todo o perioperatório
O consenso do ERAS traz, ainda, princípios importantes que afetam o cuidado do pré-operatório até o período pós-alta hospitalar, como terapia guiada por metas para manejo hemodinâmico e de fluidoterapia, analgesia poupadora de opioides, uso de bloqueios anestésicos regionais, programas de manejo de sangue (PBM, do inglês patient blood management), prevenção da fibrilação atrial e prevenção de infecção de ferida operatória.5 Aos leitores que se interessarem, vale a leitura do artigo e suas referências, quando se aprofundarem em um tema específico.
Muitas são as medidas que podem ser realizadas buscando reduzir as complicações perioperatórias e melhorar os desfechos em cirurgia cardíaca, otimizando a recuperação do paciente. Cabe a cada serviço identificar o conjunto de medidas que mais se adequa ao perfil de pacientes que atende e que é factível a cada realidade.
Certamente, as janelas de oportunidade de melhoria serão destacadas ao se conhecer adequadamente os resultados atuais do serviço. Além disso, a implementação das medidas seguida pela análise dos dados permitirá avaliar a efetividade do que foi implementado naquele cenário.
Referências
1Pahwa S, Bernabei A, Schaff H, Stulak J, Greason K, Pochettino A, Daly R, Dearani J, Bagameri G, King K, Viehman J, Crestanello J. Impact of postoperative complications after cardiac surgery on long-term survival. J Card Surg. 2021;36(6):2045-52. doi:10.1111/jocs.15471.
2Mejia OA, Lisboa LA, Caneo LF, Arita ET, Brandão CM, Dias RR, Costa R, Jatene MB, Pomerantzeff PM, Dallan LA, Jatene FB. Analysis of >100,000 cardiovascular surgeries performed at the heart institute and a new era of outcomes. Arq Bras Cardiol [Internet]. 2020 Apr;114(4):603-12. doi: 10.36660/abc.20190736.
3Ferguson TB Jr, Peterson ED, Coombs LP, Eiken MC, Carey ML, Grover FL, DeLong ER. Use of continuous quality improvement to increase use of process measures in patients undergoing coronary artery bypass graft surgery: a randomized controlled trial. JAMA. 2003;290(1):49‐56. doi: 10.1001/jama.290.1.49.
4Demetriou C, Hu L, Smith TO, Hing CB. Hawthorne effect on surgical studies. ANZ J Surg. 2019;89(12):1567-76. doi: 10.1111/ans.15475.
5Grant MC, Crisafi C, Alvarez A, Arora RC, Brindle ME, Chatterjee S, Ender J, Fletcher N, Gregory AJ, Gunaydin S, Jahangiri M, Ljungqvist O, Lobdell KW, Morton V, Reddy VS, Salenger R, Sander M, Zarbock A, Engelman D. Perioperative care in cardiac surgery: a joint consensus statement by the Enhanced Recovery After Surgery (ERAS) Cardiac Society, ERAS International Society, and The Society of Thoracic Surgeons (STS) [published correction appears in Ann Thorac Surg. 2024 Aug;118(2):524-5. doi: 10.1016/j.athoracsur.2024.06.006]. Ann Thorac Surg. 2024;117(4):669-89. doi: 10.1016/j.athoracsur.2023.12.006.
6Marmelo F, Rocha V, Moreira-Gonçalves D. The impact of prehabilitation on post-surgical complications in patients undergoing non-urgent cardiovascular surgical intervention: Systematic review and meta-analysis [published correction appears in Eur J Prev Cardiol. 2018 Jun;25(9):NP2. doi: 10.1177/2047487318777961]. Eur J Prev Cardiol. 2018;25(4):404-17. doi: 10.1177/204748731775237399.
7Arora RC, Brown CH 4th, Sanjanwala RM, McKelvie R. “NEW” prehabilitation: a 3-way approach to improve postoperative survival and health-related quality of life in cardiac surgery patients. Can J Cardiol. 2018;34(7):839-49. doi: 10.1016/j.cjca.2018.03.020.
8American Society of Anesthesiologists. Practice guidelines for preoperative fasting and the use of pharmacologic agents to reduce the risk of pulmonary aspiration: application to healthy patients undergoing elective procedures: an updated report by the American Society of Anesthesiologists Task Force on Preoperative Fasting and the Use of Pharmacologic Agents to Reduce the Risk of Pulmonary Aspiration. Anesthesiology. 2017;126:376-93. doi: 10.1097/ALN.0000000000001452.
9Smith I, Kranke P, Murat I, Smith A, O’Sullivan G, Søreide E, Spies C, in’t Veld B; European Society of Anaesthesiology. Perioperative fasting in adults and children: guidelines from the European Society of Anaesthesiology. Eur J Anaesthesiol. 2011;28(8):556-69. doi: 10.1097/EJA.0b013e3283495ba1.
10Umesh G, Tejesh CA. Probing the future – Can gastric ultrasound herald a change in perioperative fasting guidelines? Indian J Anaesth. 2018;62(10):735-7. doi: 10.4103/ija.IJA_669_18.
11MacKay EJ, Zhang B, Augoustides JG, Groeneveld PW, Desai ND. Association of intraoperative transesophageal echocardiography and clinical outcomes after open cardiac valve or proximal aortic surgery. JAMA Netw Open. 2022;5(2):e2147820. doi: 10.1001/jamanetworkopen.2021.47820.
12Metkus TS, Thibault D, Grant MC, Badhwar V, Jacobs JP, Lawton J, O’Brien SM, Thourani V, Wegermann ZK, Zwischenberger B, Higgins R. Transesophageal echocardiography in patients undergoing coronary artery bypass graft surgery. J Am Coll Cardiol. 2021;78(2):112-22. doi: 10.1016/j.jacc.2021.04.064.
13Zochios V, Klein AA, Gao F. Protective invasive ventilation in cardiac surgery: a systematic review with a focus on acute lung injury in adult cardiac surgical patients. J Cardiothorac Vasc Anesth. 2018;32(4):1922-36. doi: 10.1053/j.jvca.2017.10.031.
14Mathis MR, Duggal NM, Likosky DS, Haft JW, Douville NJ, Vaughn MT, Maile MD, Blank RS, Colquhoun DA, Strobel RJ, Janda AM, Zhang M, Kheterpal S, Engoren MC. Intraoperative mechanical ventilation and postoperative pulmonary complications after cardiac surgery. Anesthesiology. 2019;131(5):1046-62. doi: 10.1097/ALN.0000000000002909.
15Bignami E, Andrei G. Pro: mechanical ventilation during cardiopulmonary bypass in adult cardiac surgery. J Cardiothorac Vasc Anesth. 2024;38(4):1041-4. doi: 10.1053/j.jvca.2024.01.004.
16Zorrilla-Vaca A, Healy R, Grant MC, Joshi B, Rivera-Lara L, Brown C, Mirski MA. Intraoperative cerebral oximetry-based management for optimizing perioperative outcomes: a meta-analysis of randomized controlled trials. Can J Anaesth. 2018;65(5):529-42. doi: 10.1007/s12630-018-1065-7.
17Gan TJ, Belani KG, Bergese S, Chung F, Diemunsch P, Habib AS, Jin Z, Kovac AL, Meyer TA, Urman RD, Apfel CC, Ayad S, Beagley L, Candiotti K, Englesakis M, Hedrick TL, Kranke P, Lee S, Lipman D, Minkowitz HS, Morton J, Philip BK. Fourth Consensus Guidelines for the Management of Postoperative Nausea and Vomiting. Anesth Analg. 2020;131(2):411-48. doi: 10.1213/ANE.0000000000004833.
18Magruder JT, Weiss SJ, DeAngelis KG, Haddle J, Desai ND, Szeto WY, Acker MA; Penn Perfusion Team Working Group. Correlating oxygen delivery on cardiopulmonary bypass with Society of Thoracic Surgeons outcomes following cardiac surgery. J Thorac Cardiovasc Surg. 2022;164(3):997-1007. doi: 10.1016/j.jtcvs.2020.12.008.
19Flynn BC, He J, Richey M, Wirtz K, Daon E. Early extubation without increased adverse events in high-risk cardiac surgical patients. Ann Thorac Surg. 2019;107:453-9. doi: 0.1016/j.athoracsur.2018.09.034.
20Gershengorn HB, Wunsch H, Hua M, Bavaria JE, Gutsche J. Association of overnight extubation with outcomes after cardiac surgery in the intensive care unit. Ann Thorac Surg. 2019;108:432-42. doi: 10.1016/j.athoracsur.2019.04.013.
21Badhwar V, Esper S, Brooks M, Milikutla S, Hardison R, Mallion D, Chu D, Wei L, Subramaniam K. Extubating in the operating room after adult cardiac surgery safely improves outcomes and lowers costs. J Thorac Cardiovasc Surg. 2014;148:3101-9.e1. doi: 10.1016/j.jtcvs.2014.07.037.
22Dorsa AG, Rossi AI, Thierer J, Lupiañez B, Vrancic JM, Vaccarino GN, Piccinini F, Raich H, Bonazzi SV, Benzadon M, Navia DO. Immediate extubation after off-pump coronary artery bypass graft surgery in 1,196 consecutive patients: feasibility, safety and predictors of when not to attempt it. J Cardiothorac Vasc Anesth. 2011;25(3):431-6. doi: 10.1053/j.jvca.2010.08.013.
23Zarbock A, Küllmar M, Ostermann M, Lucchese G, Baig K, Cennamo A, Rajani R, McCorkell S, Arndt C, Wulf H, Irqsusi M, Monaco F, Di Prima AL, García Alvarez M, Italiano S, Miralles Bagan J, Kunst G, Nair S, L’Acqua C, Hoste E, Vandenberghe W, Honore PM, Kellum JA, Forni LG, Grieshaber P, Massoth C, Weiss R, Gerss J, Wempe C, Meersch M. Prevention of cardiac surgery-associated acute kidney injury by implementing the KDIGO guidelines in high-risk patients identified by biomarkers: the PrevAKI-multicenter randomized controlled trial. Anesth Analg. 2021 Aug 1;133(2):292-302. doi: 10.1213/ANE.0000000000005458.