A fibrilação atrial (FA) é a causa mais comum de disritmia cardíaca, afetando 32 milhões de pessoas no mundo. A FA também é uma complicação comum após uma cirurgia cardíaca (10-65%), estando associada a um risco significativo de acidente vascular encefálico (AVE), insuficiência cardíaca congestiva e mortalidade, tanto no período perioperatório quanto no pós-operatório tardio. O apêndice atrial esquerdo (AAE) é o local de origem mais frequente de trombo em pacientes com FA que sofreram AVE. Atualmente, a anticoagulação oral (ACO) com varfarina ou anticoagulantes orais diretos é o tratamento de escolha para a prevenção de AVE e tromboembolismo sistêmico em pacientes com FA, com escore CHA2DS2-VASc ≥ 1; a ACO mostra de maneira consistente a melhora da sobrevida. Apesar de sua eficácia já estar bem estabelecida, considera-se que uma grande porcentagem de pacientes com risco de AVE tem contraindicações absolutas ou relativas ao uso de ACO, em razão do alto risco de sangramento, da falta de adesão do paciente, das interações medicamentosas ou dos custos elevados.
O AAE possui função de reservatório de sangue e é a estrutura mais distensível no átrio esquerdo, atuando como câmara de descompressão em pacientes com aumento da pressão e do volume do átrio esquerdo. Em pacientes com FA, há remodelamento do AAE, o que resulta em seu funcionamento como uma bolsa estática com velocidades de fluxo reduzidas e redução da distensibilidade, aumentando a predisposição à formação de trombos. A FA pode levar a um comprometimento da função de condução elétrica do AAE, com uma diminuição na velocidade do fluxo dentro dele, que é um importante preditor de formação de trombo. Além disso, a FA pode causar um estado protrombótico manifestado por disfunção endotelial e ativação de fatores de coagulação. A FA de longa duração também leva a remodelamento atrial, fibrose e inflamação do endotélio do átrio esquerdo, especialmente do AAE, levando a gatilhos focais e arritmias de reentrada, contribuindo para um círculo vicioso.
As diretrizes atuais da European Society of Cardiology (2016) e da American Heart Association/American College of Cardiology (2014) têm uma recomendação Classe IIb referente à excisão cirúrgica de rotina do AAE em pacientes submetidos à cirurgia cardíaca; já a diretriz da Society of Thoracic Surgeons de 2017 tem uma recomendação Classe IIa. Existem diversas técnicas de exclusão do AAE (Figura 1), porém a amputação seguida da sutura epicárdica parece ser a estratégia mais efetiva.
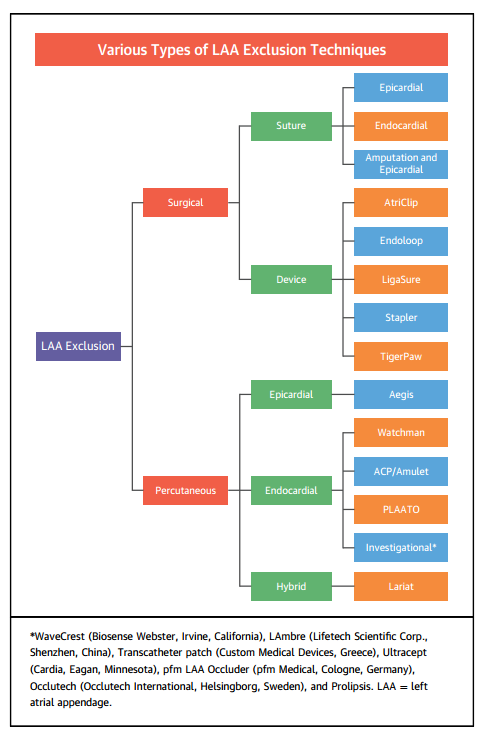
Figura 1. Técnicas de exclusão do AAE. Fonte: Turagam et al.
Até o momento, com base nos dados disponíveis, o fechamento profilático do AAE durante uma cirurgia cardíaca concomitante não é completamente recomendado. Permanece a questão de saber se existe um grupo de pacientes de alto risco que se beneficiariam do fechamento profilático do AAE concomitante a outro procedimento cardíaco. Em teoria, o grupo de pacientes com contraindicação ao ACO, alto escore do HAS-BLED ou CHA2DS2-VASc, é o grupo que se beneficiaria com a ressecção do AAE.
No entanto, neste ano, Park-Hansen et al. publicaram o estudo LAACS – Left Atrial Appendage Closure by Surgery, um estudo prospectivo, randomizado, que comparou pacientes que realizaram cirurgia cardíaca aberta eletiva (revascularização, troca de valva ou cirurgia combinada) e receberam tratamento concomitante com exclusão do AAE ou tratamento padrão, com acompanhamento de 6 anos. Como resultado, 5% dos pacientes do grupo LACCS tiveram um evento primário (AVE, ataque isquêmico transitório ou evidência de novo infarto silencioso verificada por exame de imagem), em comparação com o grupo controle, com 16% (Figura 2). Apesar disso, não houve diferença estatisticamente significante entre a mortalidade geral nos dois grupos. Assim, a exclusão do AAE parece ser um procedimento seguro, de baixo custo e de fácil execução, que pode diminuir o risco de isquemia cerebral no pós-operatório em pacientes submetidos à cirurgia cardíaca eletiva.
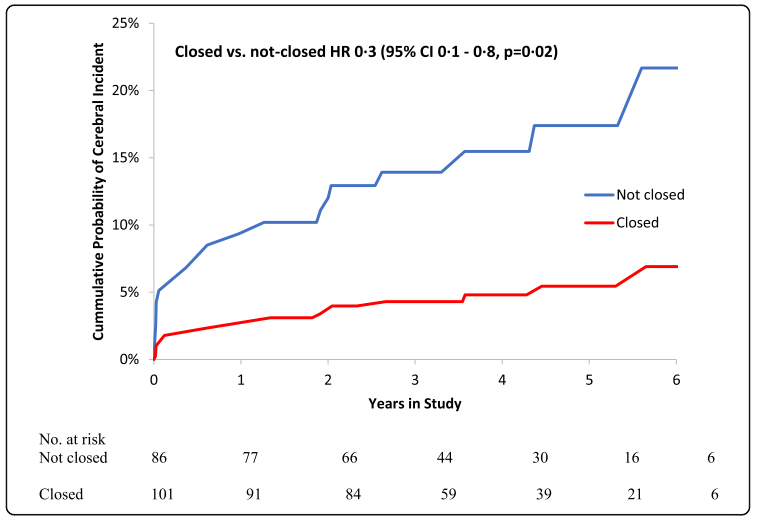
Figura 2. Probabilidade acumulada de eventos primários (AVE, ataque isquêmico transitório ou evidência de novo infarto silencioso verificada por exame de imagem) de acordo com o estudo LACCS. Fonte: Park-Hansen et al.
Referências
-
Turagam MK, Velagapudi P, Kar S, Holmes D, Reddy VY, Refaat MM, et al. Cardiovascular therapies targeting left atrial appendage. J Am Coll Cardiol. 2018 Jun 25. pii: S0735-1097(18)35139-8.
-
Schneider B, Stollberger C, Sievers HH. Surgical closure of the left atrial appendage – a beneficial procedure? Cardiology. 2005;104(3):127-32.
-
Park-Hansen J, Holme SJV, Irmukhamedov A, Carranza CL, Greve AM, Al-Farra G, et al. Adding left atrial appendage closure to open heart surgery provides protection from ischemic brain injury six years after surgery independently of atrial fibrillation history: the LAACS randomized study. J Cardiothorac Surg. 2018;13(1):53.