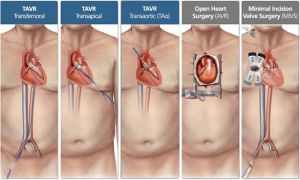
 Figura 1. Opções de acesso para troca valvar aórtica
Figura 1. Opções de acesso para troca valvar aórtica
Fonte: https://newheartvalve.com/understand-aortic-stenosis/treatment-options/
A estenose valvar aórtica apresenta prevalência crescente, principalmente pelo aumento da expectativa de vida e o consequente envelhecimento da população. As etiologias dividem-se quanto à faixa etária, sendo mais comuns nos jovens a etiologia reumática e a doença congênita bicúspide, enquanto nos idosos prevalece a doença aórtica senil calcífica, sendo relacionada a fatores de risco gerais para aterosclerose, como dislipidemia, tabagismo e hipertensão arterial sistêmica¹.
Além da troca valvar cirúrgica, os procedimentos de acesso transcateter tornaram-se uma alternativa à cirurgia em casos selecionados e individualizados, alimentando mais ainda a discussão e o estudo das repercussões da desproporção entre a prótese e a superfície corporal do paciente, que pode ser evitada com a escolha da prótese mais adequada a partir de cálculos que levam em consideração a área de superfície corporal.
O termo prosthesis-patient mismatch (PPM) em inglês, ou desproporção prótese-paciente (DPP) em português, pode ser aplicado a um espectro de variedades clínicas: prótese pequena em relação à superfície corpórea do paciente, gradiente transvalvar excessivo pós-implante, aumento do gradiente transvalvar ao esforço, orifício efetivo indexado estenótico e combinações possíveis entre essas e outras variáveis².
O mismatch protético foi formalmente discutido pela primeira vez em 1978, a partir de uma publicação de Rahimtoola³, que trouxe à tona a possibilidade das trocas valvares introduzirem novos problemas clínicos, dentre eles um problema que não era muito enfatizado até então: a desproporção entre a prótese e a área valvar indexada, podendo dificultar o enchimento e/ou o esvaziamento ventricular.
Na atualidade, com o crescimento de novas tecnologias em troca valvar aórtica transcateter, a discussão quanto ao mismatch ganhou renovada importância, sendo um tema relevante no dia a dia do cirurgião cardiovascular e que deve ser levado em consideração nos procedimentos de troca valvar aórtica, seja cirúrgico, seja transcateter. Outro fator importante é o desenvolvimento de técnicas diagnósticas e exames complementares, que, ao se tornarem cada vez mais sofisticados e acurados, aumentam o diagnóstico do mismatch e guiam o raciocínio do cirurgião quanto à melhor abordagem, à prótese mais adequada e à avaliação de necessidade de ampliação do anel valvar e da via de saída do ventrículo esquerdo.
Dois termos são usados para descrever o tamanho das próteses valvares: área efetiva do orifício indexada e área geométrica do orifício. A área efetiva do orifício indexada (AEOi) é uma das maneiras para mensurar o risco de uma prótese apresentar desproporção e é obtida a partir de um cálculo que consiste em dividir a área efetiva do orifício, um parâmetro ecocardiográfico, pela área de superfície corporal (ASC) do paciente, que é obtida pela fórmula de Mosteller (ASC = raiz quadrada (altura * peso/3.600). Se o resultado for > 0,85 cm²/m², a chance de DPP é praticamente nula, entre 0,65-0,85 cm²/m² tem-se DPP moderada e, quando o resultado for < 0,65 cm²/m², o paciente é classificado com uma DPP grave. Já a área geométrica é a área anatômica da prótese⁴.
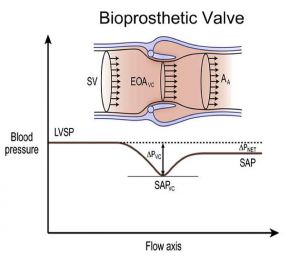
Figura 2. Análise evidenciando que o orifício efetivo (área funcional) corresponde a uma área menor em relação à área geométrica (área anatômica)².
Uma metanálise, a maior até o momento atual, foi publicada no European Journal of Cardiothoracic Surgery, com a análise de 108.182 pacientes. O estudo evidenciou que mais da metade dos pacientes submetidos à troca valvar aórtica já saem de sala com mismatch moderado ou grave. Mostrou, ainda, que o mismatch começa a ter influência na hemodinâmica do paciente já no pós-operatório imediato e que os resultados negativos e a influência na mortalidade relativos à desproporção protética podem influir na vida do paciente até 10 anos após a troca valvar⁵.
A análise quanto à prótese mais adequada tem início com o cálculo da superfície corporal do paciente. Quanto maior a superfície corporal, maior será o orifício efetivo da valva aórtica e, consequentemente, maior será a numeração da prótese a ser usada. O número obtido a partir do cálculo da superfície corporal deve ser multiplicado pela constante 0,85 cm²/m². Essa constante é a área efetiva necessária para que não haja restrição à ejeção de sangue pelo ventrículo esquerdo. É um cálculo de valor funcional, correspondendo à menor área do jato. Após os cálculos, deve-se verificar as relações dos valores com as próteses de cada fabricante, que podem diferir quanto à geometria e ao perfil.
Quando a raiz aórtica do paciente é menor que o necessário para o implante da prótese adequada, uma possibilidade de estratégia cirúrgica é a ampliação da raiz da aorta. Tal estratégia deve ser ponderada, já que há complicações cirúrgicas associadas, como danos à via de saída e bloqueios atrioventriculares. Um estudo publicado na revista Interactive CardioVascular and Thoracic Surgery⁶ analisou cerca de 13 mil pacientes comparando a troca valvar aórtica isolada e a troca valvar aórtica combinada à ampliação da raiz aórtica. Não houve diferença de mortalidade entre os dois grupos. Porém, os pacientes do grupo da cirurgia combinada tiveram menor risco de implante de uma prótese de tamanho inadequado e saíram da sala cirúrgica com orifício efetivo indexado maior, diminuindo a chance de mismatch. Ou seja, de acordo com o estudo, a ampliação da raiz aórtica é uma estratégia adequada para evitar mismatch. Porém, devem-se levar em consideração a complexidade e os riscos do procedimento cirúrgico.
Em resumo, a DPP é uma entidade de alta prevalência e com impacto associado ao aumento da mortalidade. Logo, são necessárias estratégias pré e intraoperatórias para prevenir a DPP na prótese valvar aórtica.
Referências
- Tarasoutchi F, Montera MW, Grinberg M, Barbosa MR, Piñeiro DJ, Sánchez CRM, et al. Diretriz Brasileira de Valvopatias – SBC 2011/I Diretriz Interamericana de Valvopatias – SIAC 2011. Arq Bras Cardiol 2011;97(5 supl. 1):1-67.
- Cohn LH. Cardiac surgery in the adult. 5. ed. New York: McGraw-Hill Medical; 2018.
- Rahimtoola SH. The problem of valve prosthesis-patient mismatch. Circulation. 1978;58(1):20‐24. doi: 10.1161/01.cir.58.1.20
- Zoghbi W, Chambers JB, Dumesnil JG, Foster E, Gottdiener JS, Grayburn PA, et al. Recommendations for evaluation of prosthetic valves with echocardiography and Doppler ultrasound. J Am Soc Echocardiogr. 2009;22(9):975-1014. doi: 10.1016/j.echo.2009.07.013
- Sá MPBO, de Carvalho MMB, Sobral Filho DC, Cavalcanti LRP, Rayol SC, Diniz RGS, et al. Surgical aortic valve replacement and patient–prosthesis mismatch: a meta-analysis of 108 182 patients. Eur J Cardiothorac Surg. 2019;6(1):44-54. doi: 10.1093/ejcts/ezy466
- Sá MPBO, Carvalho MMB, Sobral Filho DC, Cavalcanti LRP, Diniz RGS, Rayol SC, et al. Impact of surgical aortic root enlargement on the outcomes of aortic valve replacement: a meta-analysis of 13.174 patients. Interact Cardiovasc Thorac Surg. 2019;29(1):74-82. doi: 10.1093/icvts/ivy364