A Tetralogia de Fallot (TOF) é a forma mais comum de doença cardíaca cianótica, com uma incidência de 4 em 10.000 nascidos vivos1. Compreende uma malformação cardíaca congênita que consiste em 4 defeitos: comunicação interventricular, obstrução da via de saída do ventrículo direito, desvio do septo ventricular pela raiz aórtica e hipertrofia ventricular direita. A apresentação inicial da TOF varia dependendo da gravidade da obstrução do fluxo sanguíneo para os pulmões, sendo que a maioria dos pacientes se apresenta no período neonatal com cianose leve a moderada, mas normalmente sem dificuldade respiratória. O diagnóstico é confirmado com ecocardiografia, a partir da qual serão delineados a gravidade da obstrução subpulmonar, seu componente dinâmico, o tamanho das artérias pulmonares direita e esquerda e quaisquer fontes adicionais de fluxo de sangue para os pulmões2.Trata-se de uma doença reparável cirurgicamente.
O tratamento cirúrgico da TOF teve diferentes marcos na cirurgia cardíaca3. Em 1945, se descreveu a primeira paliação exitosa desta enfermidade, conhecida por cirurgia de Blalock-Taussig (ou Blalock-Taussig-Thomas), na qual usa-se a artéria subclávia para conectar a artéria pulmonar como uma forma de aumentar o fluxo sanguíneo pulmonar4. Hoje, utiliza-se a técnica de Blalock-Taussig modificada, na qual para se realizar o shunt, se interpõe um conduto protético entre a artéria subclávia direita e a artéria pulmonar direita3. O objetivo desse shunt é fornecer fluxo suficiente da artéria pulmonar para aliviar a cianose, mas não para causar sobrecirculação pulmonar. Na preparação para a criação de um shunt de artéria pulmonar sistêmico, uma vez que a dissecção apropriada é realizada, os vasos de derivação alvo são identificados e o enxerto de politetrafluoroetileno (PTFE) da artéria sistêmica para pulmonar é cortado nesse tamanho. Em geral, o tronco braquiocefálico e a artéria pulmonar direita são os vasos escolhidos para a criação do shunt5.
O reparo cirúrgico intracardíaco da TOF só foi relatado pela primeira vez em 19543. Tradicionalmente, a TOF foi reparada através de uma incisão do ventrículo direito (VD), proporcionando uma excelente exposição para o fechamento do defeito do septo ventricular (SVD) e alívio da obstrução do trato de saída do ventrículo direito (TSVD), mas havia preocupações de que a cicatriz resultante pudesse aumentar o incidência de arritmias ventriculares e morte súbita e comprometimento da função ventricular direita. A abordagem atrial direita (AD) só tornou-se popular na década de 80 por sua vantagem percebida de evitar os problemas associados à incisão do VD, sendo atualmente a abordagem mais utilizada5.
De forma geral, algumas questões permanecem em relação ao manejo da TOF, principalmente no que se refere à preferência do momento cirúrgico e às lesões residuais da doença. A intervenção inicial pode ser a paliativa já citada (técnica de Blalock-Taussig modificada), mas a tendência nos centros de excelência é cada vez mais para o reparo completo neonatal. O reparo completo, sempre realizado com uso de circulação extracorpórea (CEC), consiste no fechamento da comunicação interventricular (CIV) com retalho que canaliza o ventrículo esquerdo para a raiz da aorta, alívio da obstrução subpulmonar e reconstrução, se necessário, das artérias pulmonares. O acompanhamento de pacientes nascidos há 30 anos mostra uma taxa de sobrevivência superior a 85%. Os problemas crônicos que agora enfrentam esses adultos incluem regurgitação pulmonar, recorrência de estenose pulmonar e arritmias ventriculares2. Na reconstrução da TSVD, a arteriotomia pulmonar e ventriculotomia são fechadas com remendo de pericárdio autólogo (alguns cirurgiões usam enxerto tubular de Dacron ou PTFE)5(Figura 1).
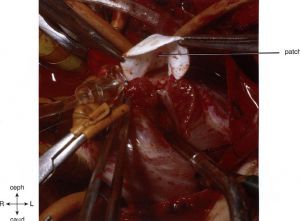
Figura 1. Um patch oval de PTFE é suturado ao longo da via de saída, começando distalmente à artéria pulmonar principal. Fonte: Litwin6
O pericárdio autólogo pode ser cortado em uma configuração de “pantalona” para eventualmente preencher os seios de Valsalva (Figura 2a). Três suturas interrompidas são colocadas no ápice inciso do remendo (para alinhar com a comissura da válvula pulmonar anterior) e amarradas. A Figura 2b mostra o patch pericárdico em formato de “pantalona” sendo suturado, ampliando a área supravalvar. A Figura 2c demonstra a técnica de coleta que ajuda a combinar o pericárdio com a parede da artéria pulmonar existente. O reparo supravalvar concluído é observado na Figura 2d5.
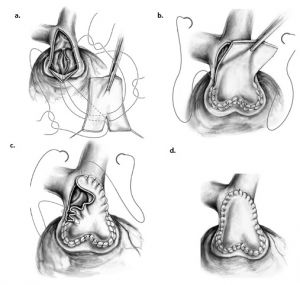
Figura 2. Reconstrução VSVD com pericárdio autólogo em forma de “pantalona”. Fonte: Mavroudis5
Contudo, se ocorrer hipertensão ventricular direita pós-reparo após saída da circulação extracorpórea (CEC), é indicado realizar um patch transanular. O paciente, então, volta pra CEC, e uma ou duas suturas interrompidas podem ser removidas sem interromper a reconstrução supravalvar. A incisão transanular é feita com a intenção de preservar as conexões comissurais da válvula pulmonar anterior. O objetivo é preservar a competência dos dois folhetos, que agora estão separados. Uma vez que a válvula é preservada e a incisão transanular de tamanho adequado para o ventrículo é realizada, então outro patch de pericárdio pode ser colocado para aumentar o original5 (Figuras 3 e 4).
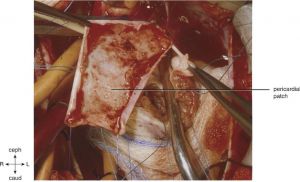 Figura 3. A incisão de ventriculotomia longitudinal alta é estendida através do anel valvar pulmonar hipoplásico e artéria pulmonar principal. Um pericárdio autólogo patch é suturado à incisão do trato de saída, iniciando a sutura contínua no artéria pulmonar principal distal. Fonte: Litwin6
Figura 3. A incisão de ventriculotomia longitudinal alta é estendida através do anel valvar pulmonar hipoplásico e artéria pulmonar principal. Um pericárdio autólogo patch é suturado à incisão do trato de saída, iniciando a sutura contínua no artéria pulmonar principal distal. Fonte: Litwin6
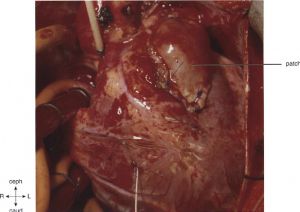
Figura 4. O aumento do reparo do patch da via de saída está completo. O tamanho do patch é grande o suficiente para evitar o bloqueio residual na via de saída, mas não é excessivo; isso pode ajudar a evitar o desenvolvimento posterior de um aneurisma de placa. Fonte: Litwin6
Um dos aspectos mais controversos da correção da TOF no primeiro ano de vida relaciona-se exatamente à necessidade de ampliação transanular da via de saída do VD7. Essa controvérsia deve-se ao fato da regurgitação pulmonar ser uma possível sequela importante. Isso é particularmente importante porque a regurgitação pulmonar residual é associada com dilatação do ventrículo direito, disfunção de ambos os ventrículos, diminuição da tolerância ao exercício e aumento do risco de arritmias8.
Ressalta-se que nessas cirurgias o desejável sempre é a preservação da valva pulmonar, porém nos casos em que isso não é possível, podem ser utilizados homoenxertos, heteroenxertos ou válvulas pulmonares de PTFE, até mesmo para tentar minimizar a regurgitação pulmonar5. Rawat et al. (2020)9 compararam os resultados à curto prazo do uso de válvula de membrana de PTFE bicúspide versus a cirurgia com apenas a reconstrução transanular com remendo de pericárdio da via de saída do ventrículo direito. Neste estudo, observou-se que apesar de alguns resultados não apresentarem significância estatística, foi possível concluir que as válvulas bicúspides de membrana de PTFE diminuem significativamente a pressão venosa central no pós-operatório imediato, facilitam a extubação precoce e, assim, evitam comorbidades relacionadas à ventilação. Tal resultado aponta a importância de uma avaliação tanto a longo prazo de estudos semelhantes, quanto dos que usam outras técnicas para fins de comparação e evolução dos procedimentos atuais afim de promover cada vez mais melhores resultados aos “pequenos pacientes”.
Referências
- Hoffman JIE, Kaplan S. A incidência de doença cardíaca congênita. J Am Coll Cardiol . 2002; 39 (12): 1890-1900. doi: 1016 / S0735-1097 (02) 01886-7
- Bailliard F, Anderson RH. Tetralogy of Fallot. Orphanet J Rare Dis. 2009 Jan 13;4:2. doi: 10.1186/1750-1172-4-2.
- Bautista-Hernández V. Tetralogía de Fallot com estenosis pulmonar: aspectos novedosos. Cir Cardiov. 2014;21(2):127–13.
- Kiran U, Aggarwal S, Choudhary A, Uma B, Kapoor PM. O shunt de blalock e taussig revisitado. Ann Card Anaesth . 2017; 20 (3): 323-330. doi: 10.4103 / aca.ACA_80_17.
- Mavroudis C, Backer CL (eds.). Atlas of pediatric cardiac surgery. London: Springer-Verlag; 2015.
- Litwin, SB. Color Atlas of Congenital Heart Surgery. London: Springer-Verlag; 2007.
- Moraes-Neto FR, Gomes CA, Lapa C, Hazin S, Tenório E, Mattos S et al. Tratamento cirúrgico da tetralogia de Fallot no primeiro ano de vida. Rev Bras Cir Cardiovasc 2000; 15( 2 ): 143-153.
- Redington AN, Oldershaw PJ, Shinebourne EA, Rigby ML. A new technique for the assessment of pulmonary regurgitation and its application to the assessment of right ventricular function before and after repair of tetralogy of Fallot. Br Heart J. 1988;60(1):57-65
- Rawat S, Jaswal V, Thingnam SKS, Singh H, Mahajan S, Kynta RL et al. Short-term outcome of Polytetrafluoroethylene Membrane Valve versus Transannular Pericardial patch Reconstruction of Right Ventricular Outflow Tract in Tetralogy of Fallot: a Randomized Controlled Trial. Braz. J. Cardiovasc. Surg. 2021; 36(1): 39-47.