Por: Prof. Dr. Domingo M. Braile
A Cirurgia Cardíaca foi durante mais de 40 anos considerada o ápice dos procedimentos cirúrgicos, ocupando um lugar de destaque entre os candidatos à residência da especialidade, concorrendo entre os melhores cérebros das universidades.
As características do ato cirúrgico, exigia profissionais altamente capazes, tanto do ponto de vista técnico, como tático, em um ambiente desafiador em que a vida dos pacientes era mantida artificialmente por equipamentos dotados de tecnologia altamente complexa, que incorporavam os conhecimentos, mais adiantados da Fisiologia e da Homeostase do metabolismo celular[1].
Os conhecimentos da fisiologia eram testados em cada intervenção, obrigando o profissional a conhecer profundamente o funcionamento do sistema circulatório e do organismo em sua totalidade.
Cada operação bem-sucedida era uma vitória recompensadora para o cirurgião, a tal ponto, que um dos mais brilhantes pioneiros da especialidade, o Prof. Denton Cooley, em uma Conferência que assisti, ter dito que: Só pelo fato do paciente deixar-se operar já representava uma grande recompensa para o cirurgião.

A história começou a mudar em 1978, quando um radiologista e cardiologista Andreas Grüntzig, ou Andreas Gruentzig, auxiliado por um engenheiro, Heinrich Hopf, miniaturizaram um cateter balão, que permitiu desobstruir artérias coronarianas estenosadas[2-9].
O conceito já existia, pois Charles Dotter juntamente com Melvin Judkins, haviam publicado em 1964 na Revista Circulation a desobstrução de artérias periféricas pela passagem de cateteres coaxiais de diâmetros progressivos, salvando da gangrena 11 pacientes com obstrução das artérias dos membros inferiores.
Estava criado o conceito de “angioplastia transluminal”[7].
Por incrível que pareça, pelas complicações no início da experiência o procedimento foi abandonado e muito criticado nos Estados Unidos onde o Dr. Dotter recebeu o cognome de “crazy Charlie”[7].
Apesar de tudo o conceito de dilatar artérias permaneceu.
O próprio Dotter e outros cirurgiões da Alemanha, como o Dr. Eberhart Zeitler pensaram em usar balões infláveis para esmagar as placas de ateroma.
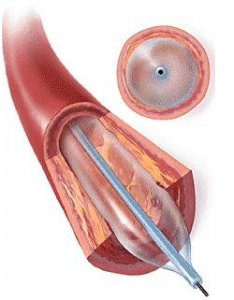
Os balões já existiam, pois, um americano Dr. Thomas Fogarty, havia criado um cateter com um balão para a realização de embolectomias[7].

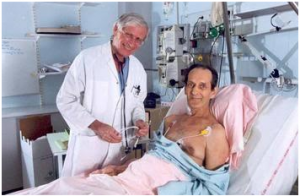
Este era o estado do tratamento das obstruções arteriais, quando surgiu uma figura carismática, que iria revolucionar o tratamento das obstruções das artérias coronarianas.
Tratava-se de uma “Tecnologia Disruptiva”
A revascularização miocárdica que representava cerca de 50% do trabalho do Cirurgião Cardíaco, passava a competir, com uma técnica menos agressiva realizada por uma simples incisão ou mesmo por punção de uma artéria periférica, sem a necessidade de anestesia ou de uma incisão transtorácica e Circulação Extracorpórea para realização dos enxertos de veia safena, anastomoses das artéria mamárias, ou outros enxertos arteriais, para os vasos coronarianos, bypassando as lesões obstrutivas.
A angioplastia coronariana desenvolvida por Grüntzig, evoluiu para novas variantes com a introdução dos “Stents” pequenas estruturas metálicas introduzidas nas artérias ao dilatá-las para evitar as reestenoses que ocorriam com frequência após algum tempo da dilatação[7].
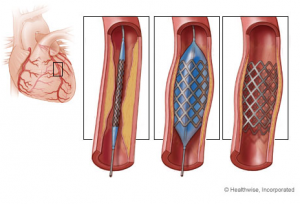
Os Stents foram sendo aperfeiçoados, eluídos com drogas para evitar proliferações celulares que provocavam estenoses.

Em 1999, pioneiramente no Brasil, o Dr. José Eduardo de Sousa[8], no Instituto Dante Pazzanese de Cardiologia, implantou o primeiro Stent, revestido com uma droga antiproliferativa, o Sirolimus, foi o emprego, “First in Man” realizado mundialmente.
Estas novas classes de Stents foram sendo aperfeiçoados, competindo de frente com as Operações de revascularização do miocárdio.
A tecnologia continua em evolução, pois, as complicações persistem, sendo a revascularização miocárdica ainda o padrão ouro nos casos mais complexos[9,10].
A dilatação das artérias coronarianas estenosadas, com balões, foi seguida do implante de Stents metálicos, para evitar as frequentes reestenoses.
Como o problema não havia sido solucionado, desenvolveram-se os Stents Farmacológicos, eluídos com drogas antiproliferativas, para aumentar a perviedade, a médio e longo prazo.
Estes procedimentos constituem o que se convencionou definir como: “Tecnologia Disruptiva”.
“Tecnologia disruptiva, é um termo que descreve a inovação tecnológica, com características que provocam uma ruptura dos padrões, modelos ou tecnologias já estabelecidos”[11].
Foi assim que as operações de revascularização miocárdica, foram sendo substituídas por um novo procedimento, sem que os Cirurgiões Cardiovasculares, tomassem ciência de que seu trabalho estava sendo ameaçado, por uma técnica menos invasiva, assimilada por outros profissionais e preferida pelos pacientes[7,8].
Como citado textualmente por Dunning (2019)[11], “… All these systems require general anesthesia and we must learn the lessons of the cardiac surgeons who were slow to enter the catheter labs and who lost the leadership in TAVI and revascularization.”
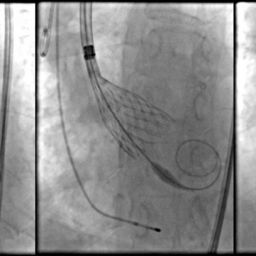
Para citar exemplos refiro-me ao implante de válvulas transcateter, que recebe a sigla de “TAVI” (Transcatheter Aortic Valve Implantation) ou “TAVR” (Transcatheter Aortic Valve Replacement) [12-14].
A substituição das válvulas cardíacas estava absolutamente estabilizada com as operações, com Circulação Extracorpórea e troca cirúrgica das válvulas estenosadas, insuficientes, ou com dupla lesão, por próteses metálicas ou biológicas.
Pacientes idosos, com estenose da válvula aórtica representavam um alto risco para suportar uma cirurgia cardíaca convencional em 2002.
Neste ano, Alain Cribier[12], após estudos em cadáveres e animais fez, na cidade de Rouen, o primeiro implante de válvula aórtica, por cateter, em um paciente portador de grave estenose aórtica calcificada, como procedimento compassivo tal o estado crítico do doente.
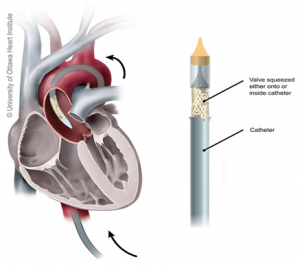
Uma prótese biológica “crimpada”(esmagada) sobre um balão foi utilizada para dilatar a válvula estenosada e ao mesmo tempo implantar a válvula no interior da válvula nativa, ancorando-a sobre os depósitos de cálcio.
Alguns outros casos foram realizados em outros pacientes compassivos (em estado quase moribundo), com resultados aceitáveis.
Poucos deram crédito a esta Técnica Disruptiva, não acreditando na sua viabilidade.
O próprio Dr. Alain Cribier, procurou-me, na época em São José do Rio Preto, para que pudesse desenvolver uma válvula de pericárdio bovino adequadamente tratado no interior do suporte por ele desenvolvido.
Fiz na época uma reunião, em que estavam presentes: o próprio Dr. Cribier, os hemodinamicistas Dr. Moacir Godoy, Dr. Luiz Antônio Gubolino e eu como cirurgião cardiovascular.
Sinceramente a técnica não nos impressionou favoravelmente.
Para colaborar com o pesquisador na Braile Biomédica® foi desenvolvida uma válvula adequada ao suporte metálico.
Uma engenheira a pedido do inventor passou um tempo na empresa para certificar-se da qualidade do procedimento.
A engenheira passou ela mesmo a produzir s válvulas no Canadá.
Nunca mais tive notícias do Dr. Cribier.
Em 2004 uma indústria multinacional, comprou os direitos da incipiente indústria liderada pelo Dr. Alain Cribier.
Desde então centenas de milhares de pacientes, atualmente mesmo de médio ou até de baixo risco, passaram a ser tratados pela nova técnica aperfeiçoada ao longo do tempo[13,14].
Um outro exemplo, ainda em desenvolvimento, é o implante de válvulas transcateter para posições mitral e tricúspide, um campo desafiador[15].
Isto tudo sem citar uma outra tecnologia disruptiva, já amplamente desenvolvida, qual seja os implantes “valve-in-valve”, que mostram resultados consistentes para reparar válvulas biológicas deterioradas, substituindo com vantagens as reoperações.
Os cirurgiões, como costuma acontecer com os profissionais que tem as ideias preconcebidas e estão desenvolvendo sua atividade em uma zona de conforto, não acreditaram nas novas técnicas, que se desenvolveram vigorosamente, a ponto de mudar o conceito de “Cirurgião Cardíaco” com a necessidade do advento de um novo profissional que resolvi denominar de “Novo Cirurgião Cardíaco” [16].
Este especialista, deverá ser capaz de manter suas atividades clássicas, e introduzir em seu portfólio também as novas tecnologias menos invasivas.
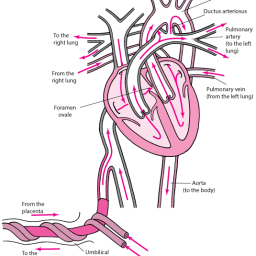
Muitas das operações para corrigir defeitos congênitos como: Comunicação interatrial (CIA), Comunicação Interventricular (CIV) Estenose da Válvula Pulmonar (EVP), Fechamento de Canal arterial persistente, e outros defeitos cardíacos vão sendo paulatinamente tratados por técnicas pouco invasivas[17].
O “Novo Cirurgião Cardiovascular” deverá ter formação muito mais ampla que aquela proporcionada pela residência estabelecida até alguns anos atrás.
Kotsis et al.[16], em seu artigo “Application of See One, Do One, Teach One Concept in Surgical Training”, afirmam: “Residents must be encouraged and given the opportunities to learn and improve upon their surgical skills by mentors who continue to improve upon their skills as well. This can all be done in an environment that keeps patient safety at the forefront”.
Vaughn A. Starnes, presidente da American Association for Thoracic Surgery (AATS), comemorando a significativa data do 100th Annual Meeting, reafirma os princípios que nortearam sua fundação no início do século passado[18].
- Build a resource that studies the disease and improves outcome measures.
- Simplify data collection to improve the accuracy and quality of the data.
- Serve all areas of the specialty, as well as multidisciplinary areas.
- Give contributors access to their own data.
- Provide a collaborative space for surgeons around the world to engage.

Espero que os cirurgiões cardiovasculares e os residentes de cirurgia cardiovascular possam assimilar as mensagens aqui especificadas, ampliando seus conhecimentos para tratamento dos pacientes cardiopatas, com todo conjunto de técnicas atuais e futuras.
REFÊRENCIAS
- Brito I, Haddad Junior H. A formulação do conceito de homeostase por Walter Cannon. Filosofia e História da Biologia [Internet]. 2017 [cited 2019 Oct 16];12:111-25. Available from: http://www.abfhib.org/FHB/FHB-12-1/FHB-12-01.pdf.
- Gruentzig A, Turina M, Schneider J. Experimental percutaneous dilatation of coronary artery stenosis. Circulation. 1976;54:II-81. doi: 10.1007/bf01468977.
- Gruentzig A, Myler R, Hanna E, Turina M. Coronary transluminal angioplasty [abstract]. Circulation. 1977;55-56(Supl III):III-84.
- Gruntzig A. Transluminal dilatation of coronary-artery stenosis. Lancet. 1978;1(8058):263. doi: 10.1016/S0140-6736(78)90500-7.
- Myler R, Gruentzig A, Stertzer S. Coronary angioplasty. In: Rapaport E, editor. Cardiology Update 1983. New York: Elsevier; 1983. p. 1-66.
- Gruentzig A, Senning A, Siegenthaler W. Nonoperative dilatation of coronary artery stenosis: percutaneous transluminal coronary angioplasty (PTCA). N Engl J Med. 1979;301:61-8. doi: 10.1056/NEJM197907123010201.
- Gottschall CAM. 1929-2009: 80 anos de cateterismo cardíaco uma história dentro da história. Rev Bras Cardiol Invas. 2009;17(2):246-68. doi: 10.1590/S2179-83972009000200019.
- Sousa JE, Costa MA, Abizaid A, Abizaid AS, Feres F, Pinto IM, et al. Lack of neointimal proliferation after implantation of sirolimus-coated stents in human coronary arteries: a quantitative coronary angiography and three-dimensional intravascular ultrasound study. Circulation. 2001;103:192-5. doi: 10.1161/01.cir.103.2.192.
- Gaudino M, Bakaeen FG, Benedetto U, Di Franco A, Fremes S, Glineur D, et al. Arterial grafts for coronary bypass. A critical review after the publication of ART and RADIAL. Circulation. 2019;140(15):127384. doi: 10.1161/CIRCULATIONAHA.119.041096.
- Godoy LC, Rao V, Farkouh ME. Coronary revascularization of patients with diabetes mellitus in the setting of acute coronary syndromes. Circulation. 2019;140:12335. doi: https://doi.org/10.1161/CIRCULATIONAHA.119.040683.
- Dunning J. Disruptive technology will transform what we think of as robotic surgery in under ten years. Ann Cardiothorac Surg. 2019;8(2):274-8. doi: 10.21037/acs.2019.03.02.
- Cribier A. The development of transcatheter aortic valve replacement (TAVR). Glob Cardiol Sci Pract. [Internet] 2016 Dec 30. [cited 2019 Oct 11];2016(4):e201632. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5624190/. doi: 10.21542/gcsp.2016.32.
- Dalby M. State of the art in TAVI: A revolution in patient care is taking place, but there is much still to learn as discussed by Dr Miles Dalby. Eur Heart J. 2018 Jun 1;39(21):1878-81. doi: 10.1093/eurheartj/ehy213.
- Mack MJ, Leon MB, Thourani VH, Makkar R, Kodali SK, Russo M, et al. Transcatheter aortic-valve replacement with a balloon-expandable valve in low-risk patients (PARTNER 3 Trial). N Engl J Med. 2019 May 2;380(18):1695-705. doi: 10.1056/NEJMoa1814052.
- Piazza N. Interventional perspectives on TMVR: what are the design issues? [slides]. Chicago: TVT 2019 CRF; 2019. Available from: https://www.tctmd.com/slide/interventional-perspectives-tmvr-what-are-design-issues.
- Kotsis SV, Chung KC. Application of see one, do one, teach one concept in surgical training. Plast Reconstr Surg. 2013; 131(5):1194-201. doi: 10.1097/PRS.0b013e318287a0b3.
- Farooqi M, Stickley J, Dhillon R, Barron DJ, Stumper O, Jones TJ, et al. Trends in surgical and catheter interventions for isolated congenital shunt lesions in the UK and Ireland. Heart. 2019;105:1103-8. doi: 10.1136/heartjnl-2018-314428.
- Starnes VA. President’s message [Internet] [cited 2019 Oct 12]. Available from: https://www.aats.org/aatsimis/AATSWeb/Association/About/President_Message.aspx.